
某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。

(1)图中试剂①~⑤溶质的化学式分别是:
①__________,②__________,③__________,④__________
⑤_____ _____。
_____。
(2)图中现象a、b、c表明检验出的离子分别是:
a__________、b__________、c__________。
(3)白色沉淀A加试剂②反应的离子方程式是____________________________
__________________。
(4)无色溶液C加试剂③的主要目的是_________________________________
______________________________。
(5)白色沉淀A若加试剂③而不加试剂②,对实验的影响是___________________________________________
 ________。
________。
(6)气体E通入试剂④发生反应的离子方程式是__________________________
____________________________。
解析 此题中要求限定试剂检验出各种阴离子,既要注意各种被检离子的特征反应,又要注意它们之间的相互干扰,然后再仔细分析。加过量试剂①得白色沉淀A,A加过量试剂②,检出两种阴离子,说明沉淀A中含两种物质,显然试剂①不会是AgNO3溶液,应为Ba(NO3)2溶液,沉淀A含BaSO4、BaSO3。试剂②应为盐酸,气体E为SO2,试剂④为溴水,a为检出SO32-;沉淀B为BaSO4,试剂③为HNO3,b为检出SO42-。无色溶液C中含阴离子OH-、
Cl-、NO3-,先加过量③(HNO3)酸化,再加试剂⑤(AgNO3溶液),c为检出Cl-。(5)白色沉淀A如加③(HNO3),则BaSO3会被氧化为BaSO4,最后按如上步骤检不出SO32-。
答案 (1)①Ba(NO3)2 ②HCl ③HNO3 ④Br2 ⑤AgNO3
(2)SO32- SO42- Cl-
(3)BaSO3+2H+===Ba2++SO2↑+H2O
(4)中和OH-,防止对Cl-的检验产生干扰
(5)会使SO32-对SO42-的检验产生干扰,不能确定SO42-和SO32-是否存在
(6)SO2+Br2+2H2O===4H++SO42-+2Br-


科目:高中化学 来源: 题型:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
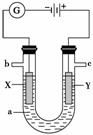
(1)若X、Y是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞,则:
①电解池中X极上的电极反应式是_______________________________________,
在X极附近观察到的现象是______________________________________________。
②Y电极上的电极反应式是_________ _____________________________________,
_____________________________________,
检验该电极反应产物的方法是_____________________________________________。
(2)若用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是_______________________________________________________,
电极反应式是__________________________________________________________。
②Y电极的材料是______________________________________________________,
电极反应式是___________________________________________________________
(说明:杂质发生的电极反应不必写出)。
③当电路中有0.04 mol电子通过时,阴极增重_____________________________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
为检验某卤代烃中的卤元素,进行如下操作,正确的顺序是
①加热②加入 溶液③取少量该卤代烃④加入足量稀硝酸酸化
溶液③取少量该卤代烃④加入足量稀硝酸酸化
⑤加入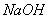 溶液⑥冷却
溶液⑥冷却
A. ③①⑤⑥②④ B. ③⑤①⑥④② C. ③②①⑥④⑤ D. ③⑤①⑥②④
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]·3H2O。42.2 g K4[Fe(CN)6]·3H2O样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示。
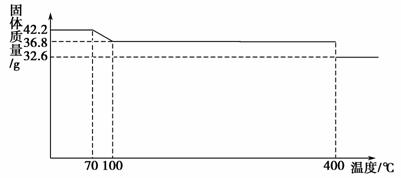
试回答下列问题:
(1) 试确定150 ℃时固体物质的化学式_________________________________
_________ ______________
______________ __________________________________________。
__________________________________________。
(2) 查阅资料知:虽然亚铁氰化钾自身毒性很低,但其水溶液与酸反应放出极毒的氰化氢(HCN)气体;亚铁氰化钾加热至一定温度时能分解产生氰化钾(KCN)。据此判断,烹饪食品时应注意的问题为_______________________________________________________________________________________
________________________________________________________________。
(3) 在25 ℃时,将a mol·L-1的KCN溶液与0.01 mol·L-1的盐酸等体积混合,反应达到平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a________0.01 mol·L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=__________________________________________
________________________________________________________________。
(4)在Fe2+、Fe3+的催化作用下,可实现2SO2+ O2+2H2O===2H2SO4的转化。已知,含SO2的废气通入含Fe2+、Fe3+的溶液中时,其中一个反应的离子方程式为4Fe2++O2+4H+===4Fe3++2H2O,则另一个反应的离子方程式为________________________________________________________________________。
O2+2H2O===2H2SO4的转化。已知,含SO2的废气通入含Fe2+、Fe3+的溶液中时,其中一个反应的离子方程式为4Fe2++O2+4H+===4Fe3++2H2O,则另一个反应的离子方程式为________________________________________________________________________。
上述转化的重要意义在于___________________________________________
________________________________________________________________。
(5)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36。室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为3时,通过计算说明Fe3+是否沉淀完全____________________________________________________________________________________________________________________________________。
(提示:当某离子浓度小于10-5 mol·L-1时可以认为该离子沉淀完全)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列涉及离子方程式书写的评价合理的是 ( )。
| 选项 | 化学反应及离子方 | 评价 |
| A | 次氯酸钙溶液中通入足量SO2:Ca2++ClO- | 正确 |
| B | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+4H++2Cl- | 错误,H+、Cl-的化学计量数应相等 |
| C | 硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O===Fe(OH)3(胶体)+3NH4+ | 错误,Fe(OH)3应该是沉淀 |
| D | 铝溶于碳酸中:2Al+3H2CO3===2Al3++3H2↑+3CO32- | 正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中的四种物质,用一种试剂即可鉴别的是( )
A. 甲酸、乙酸、甲酸钠溶液、乙酸乙酯 B.乙烯、乙烷、乙炔、丙烯
C.苯酚、乙醇、苯、四氯化碳 D.苯乙烯、苯酚、乙苯、甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
在O.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH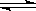 CH3COO-+H+。对于该平衡,下列叙述正确的是( )
CH3COO-+H+。对于该平衡,下列叙述正确的是( )
A.加入少量NaOH固体,平衡向正反应方向移动
B.加水,反应速率增大,平衡向逆反应方向移动
C滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com