
科目:高中化学 来源: 题型:


 AlO2-+H++H2O
AlO2-+H++H2O AlO2-+H++H2O
AlO2-+H++H2O查看答案和解析>>
科目:高中化学 来源: 题型:
现有3种化合物A、B、C均含短周期元素R,其转化关系如下图所示。
![]()
(1)若A由第三周期2种元素组成。常温下,0.1 mol/L X溶液的pH=13,则R在周
期表中的位置是 ,X中阴离子的电子式是 ,B转化为C的离子方程式是 。
(2) 若常温下A、B、C、X均为气态物质,1 mol A中含有共价键的数目约为1.806×1024, X为单质,A与X反应生成B的化学方程式是 ;在一定条件下,
A可与C反应消除C对大气的污染,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年北京市西城区高三上学期期末考试化学试卷 题型:填空题
现有3种化合物A、B、C均含短周期元素R,其转化关系如下图所示。
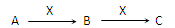
(1)若A由第三周期2种元素组成。常温下,0.1 mol/L X溶液的pH=13,则R在周
期表中的位置是 ,X中阴离子的电子式是 ,B转化为C的离子方程式是 。
(2) 若常温下A、B、C、X均为气态物质,1 mol A中含有共价键的数目约为1.806×1024, X为单质,A与X反应生成B的化学方程式是 ;在一定条件下,
A可与C反应消除C对大气的污染,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2010年山东省临沂市高考化学一模试卷(解析版) 题型:解答题
查看答案和解析>>
科目:高中化学 来源:山东省临沂市2010届高三一模(化学) 题型:填空题
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B元素的最高价氧化物的水化物与其氢化物能相互反应生成盐;A元素与C元素可形成两种液态化合物,其原子个数比分别为1:1和2:1,旦分子中电子总数分别为18和10;D元素的主族序数等于其周期数;E元素原子的最外层电子数是其电子层数的2倍。
(1)写出D元素的原子结构示意图 ;E元素在周期表中位置
(2)C和E两种元素相比较,非金属性较强的是(填元素符号) ,可以验证该结论的是 (填写编号)
A.比较这两种元素的常见单质的沸点 B.比较这两种元素的单质与氢气化合的难易
C.比较这两种元素的气态氢化物的稳定性
(3)写出D的氢氧化物在水中发生酸式电离的电离方程式:
欲使上述体系中D的简单阳离子浓度增加,可加入的物质是
(4)B元素与C元素形成的化合物中,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的B的含氧酸盐的化学式是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com