
【题目】下列物质之间的关系,错误的是:
A.CH3CH2OH和CH3OCH3互为同分异构体
B.干冰和冰为同一种物质
C.O2和O3互为同素异形体
D.CH3CH3和CH3CH2CH3互为同系物
科目:高中化学 来源: 题型:
【题目】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ⑥ | ⑦ |
| |||||
三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
四 | ② | ④ | ⑨ |
(1) 11种元素中,化学性质最不活泼的是________。(填元素符号,下同)
(2) ①②⑤中,最高价氧化物对应的水化物碱性最强的是________。(填对应的碱)
(3) ②③④中形成的简单离子半径由大到小的顺序是________________________。(填离子)
(4) 元素⑦的氢化物分子式为________,该氢化物与元素⑧的单质反应的离子方程式是______ 。
(5) ①和⑨的最高价氧化物对应的水化物的化学式为__________和________。①和⑨两元素形成化合物的化学式为____,该化合物的水溶液与元素⑧的单质反应的离子方程式为__________。
(6) ①和⑤最高价氧化物对应的水化物相互反应的化学方程式为________________。
(7) ⑧⑨![]() 三种元素形成的气态氢化物最稳定的是______________________。
三种元素形成的气态氢化物最稳定的是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,请参照元素①﹣⑩在表中的位置回答下列问题.
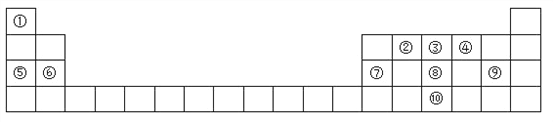
(1)画出⑩的原子结构示意图:______
(2)③、④、⑧的气态氢化物稳定性由小到大的顺序是:______(填化学式)
(3)⑧、⑨的最高价氧化物对应水化物的酸性强弱顺序是:______(填化学式)
(4)②、④两元素形成的AB2型物质的电子式是:______
(5)①、④、⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的化学式:______
(6)写出⑦的单质与⑤的最高价氧化物对应水化物反应的离子方程式:______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问題:
(1)乙二醇与灼热的氧化铜反应的方程式:__________________________________。
(2)葡萄糖可以和醋酸在一定条件下发生酯化反应,则1摩尔葡萄糖最多可以消耗________摩尔醋酸。
(3)已知乳酸的结构简式为![]() 。试回答:
。试回答:
①乳酸分子中含有_______和_________两种官能团(写名称)(此空各1分) ;
②乳酸与足量金属钠反应的化学方程式为______________________________________;
③已知两分子乳酸可在一定条件下反应生成环状的酯,写出该反应的方程式__________________。
(4)分子式为C6H12的某烃,其所有的碳原子都一定在同一平面上,则该烃的结构筒式为___________。
(5)某苯的同系物分子式为C11H16,苯环上只有一个取代基,其同分异构体共有_________种。
(6)分子中含有25个共价键的烷烃的分子式为_________,其同分异构休中沸点最低的系统名称是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量的说法不正确的是
A.煤燃烧是化学能转化为热能的过程
B.化石燃料和植物燃料燃烧时放出的能量最初均来源于太阳能
C.催化剂可以降低反应的活化能,从而改变化学反应的焓变
D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成化学能的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列说法中正确的是( )
A.122.5 g KClO3中含Cl-数目为NA
B.1 mol·L-l的NaOH溶液中含Na+数目为NA
C.标准状况下,22.4L水中含氢原子数目为2NA
D。常温常压下,32 g SO3中含氧原子数目为1.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏伽德罗常数的值,下列说法正确的是
A. 1L 1mol·L-1的NaClO溶液中含有ClO-的数目为NA
B. 78g苯中含有C=C键的数目为3NA
C. 7.8gNa2O2固体中含有的离子总数为0.3NA
D. 标准状况下,将分子总数为NA的NO和O2充分混合后,所得混合气体的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1000mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.1000mol·L-1的两种一元酸HX、HY溶液,滴定曲线如图所示。下列说法正确的是
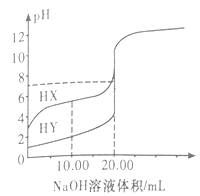
A. HX是强酸,HY是弱酸
B. V[NaOH(aq)]=10.00mL时,
C. V[NaOH(aq)]=20.00mL时,所得的两种溶液的pH均等于7
D. V[NaOH(aq)]=20.00mL时,所得的两种溶液的导电性,HX的比HY的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识的回答:
(1)浓度为0.1mol/L的8种溶液:①HNO3 ②H2SO4 ③HCOOH ④Ba(OH)2 ⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl 溶液pH值由小到大的顺序是(填写编号)____________。
(2)B为0.1molL-1NaHCO3溶液,实验测得NaHCO3溶液的pH>7,请用离子方程式表示其原因:___________________。
(3)在0.10 molL-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=___________(已知Ksp[Cu(OH) 2]=2.2x10-20)。若在0.10 molL-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com