
科目:高中化学 来源:不详 题型:实验题
| 实验操作 | 预期现象和结论 |
| | |
| | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
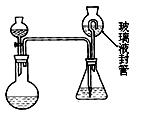
 某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量与样品质量的比值来衡量)。请回答下列问题:
某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量与样品质量的比值来衡量)。请回答下列问题: (1)为证实“稳定性二氧化氯溶液”中含有钠离子,其正确的操作步骤是: 。
(1)为证实“稳定性二氧化氯溶液”中含有钠离子,其正确的操作步骤是: 。 (2)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取mg(2g左右)
(2)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取mg(2g左右) 试样,置于烧瓶中,向分液漏斗中加入10mL盐酸溶液;②在锥形瓶中加入4g碘化钾,用100mL水溶解后,再加3mL硫酸溶液;③在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定至蓝色消失(I2+2S2O32-=2I- +S4O62-),共用去VmL硫代硫酸钠溶液。
试样,置于烧瓶中,向分液漏斗中加入10mL盐酸溶液;②在锥形瓶中加入4g碘化钾,用100mL水溶解后,再加3mL硫酸溶液;③在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定至蓝色消失(I2+2S2O32-=2I- +S4O62-),共用去VmL硫代硫酸钠溶液。 方程式为:
方程式为: 二氧化氯被还原为氯离子,该反应的离子方程式为: 。
二氧化氯被还原为氯离子,该反应的离子方程式为: 。 (Ⅱ)装置中玻璃液封管的作用是: ;如何确定烧瓶中
(Ⅱ)装置中玻璃液封管的作用是: ;如何确定烧瓶中 的二氧化氯全部被锥形瓶中的液体吸收 。
的二氧化氯全部被锥形瓶中的液体吸收 。 (Ⅲ)“稳定性二氧化氯溶液”中,ClO2的质量分数为
(Ⅲ)“稳定性二氧化氯溶液”中,ClO2的质量分数为  (用m、c、V表示)。
(用m、c、V表示)。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
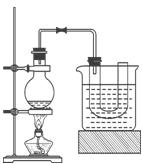
| A.氢氧化钠稀溶液 | B.碳酸钠稀溶液 |
| C.硝酸银溶液 | D.四氯化碳 |
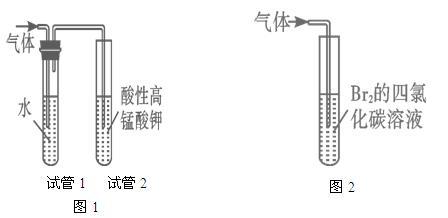
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
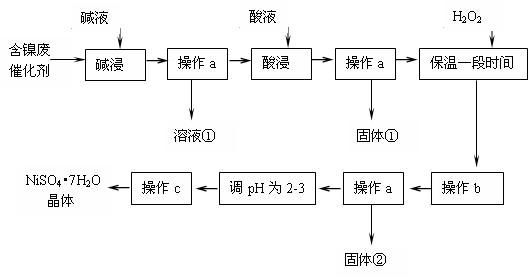
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
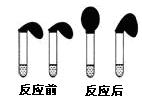
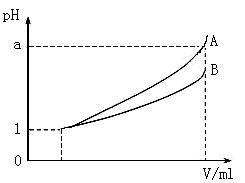
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
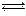 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/mol?L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
| A.2v(NH2)=v(CO2) | B.密闭容器中总压强不变 |
| C.密闭容器中混合气体的密度不变 | D.密闭容器中氨气的体积分数不变 |
 NH4HCO2+NH3?H2O
NH4HCO2+NH3?H2O
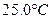 时,0-6min 氨基甲酸铵水解反应的平抑速率 ______。
时,0-6min 氨基甲酸铵水解反应的平抑速率 ______。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3COOH+Cu2O↓+2H2O”提出了质疑,并进行如下探究:
CH3COOH+Cu2O↓+2H2O”提出了质疑,并进行如下探究: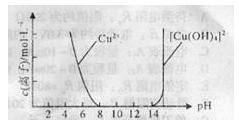
 CH3COOH+Cu2O↓+2H2O”质疑的理由:
CH3COOH+Cu2O↓+2H2O”质疑的理由:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
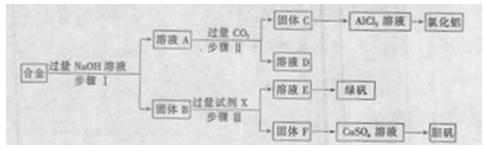
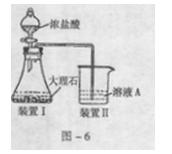
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com