
����Ŀ����ʯ���ѽ����A�ɺϳɶ��ֲ����F��һ�ֳ�Ϊ�������������ɱ����������ͼ��A�ϳ�һЩ�л������ת����ϵ��
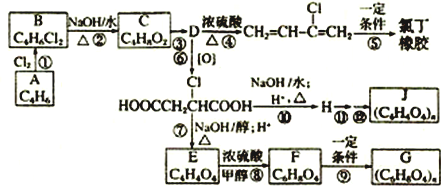
��1��������Ӧ�����ڼӳɷ�Ӧ����___________��������ţ�
��2��1H�˴Ź�����ͼ����A����ֻ�����ֻ�ѧ������ͬ����ԭ�ӣ���������о�����A�����к�������̼̼˫������д��D�Ľṹ��ʽ�� _____________ ��
��3��д��Bת��ΪC�Ļ�ѧ����ʽ__________________________________________��
��4��H������Ũ��������¿ɷֱ�����һ�ֺ���Ԫ������Ԫ������Ԫ���IJ��д��������Ԫ������Ļ�ѧ����ʽ______________________________________��
��5��д����A��Ϊͬ���칹�壬�ҷ�������4��̼ԭ�ӹ�ֱ�ߵ��л���Ľṹ��ʽ�� ____________��
��6������۲�ϳ�·��C��E���ش������������⣺
a.��C ��E�����ˢۢޢ�������Ӧ��������һ�����У���������ԭ����______________��
b.��������HOOC��CH2CHClCOOH�Ĺ����л����м�������ɣ�������м������Լ���______��
���𰸡� �٢� HOCH2CH2CHClCH2OH ClCH2CH==CHCH2Cl+2NaOH![]() HOCH2CH==CHCH2OH+2NaCl
HOCH2CH==CHCH2OH+2NaCl 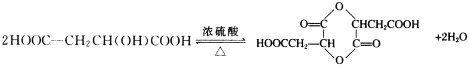 CH3
CH3![]() CCH3 �ǻ��ڱ��������Ȼ���ͬʱ��̼̼˫��Ҳ�ᱻ������Ϊ�˷�ֹ̼̼˫���������� ����������ͭ����Һ����������Һ��
CCH3 �ǻ��ڱ��������Ȼ���ͬʱ��̼̼˫��Ҳ�ᱻ������Ϊ�˷�ֹ̼̼˫���������� ����������ͭ����Һ����������Һ��
��������������Ҫ�����л���Ľṹ��������
��1��������Ӧ�����ڼӳɷ�Ӧ���Ǣ٢ۡ�
��2����D�����������֪D�Ľṹ��ʽ��HOCH2CH2CHClCH2OH��
��3��A��1,3������ϩ��BΪClCH2CH==CHCH2Cl��Bת��ΪC�Ļ�ѧ����ʽΪClCH2CH==CHCH2Cl+2NaOH![]() HOCH2CH==CHCH2OH+2NaCl��
HOCH2CH==CHCH2OH+2NaCl��
��4��H������Ũ��������¿ɷֱ�����һ�ֺ���Ԫ������Ԫ������Ԫ���IJ��������Ԫ������Ļ�ѧ����ʽΪ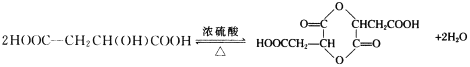 ��
��
��5��̼̼������̼ԭ������ԭ����һ��ֱ��������A��Ϊͬ���칹�壬�ҷ�������4��̼ԭ�ӹ�ֱ�ߵ��л���Ľṹ��ʽ��CH3![]() CCH3��
CCH3��
��6��a.��C��E�����ˢۢޢ�������Ӧ��������һ�����У���������ԭ�����ǻ��ڱ��������Ȼ���ͬʱ��̼̼˫��Ҳ�ᱻ������Ϊ�˷�ֹ̼̼˫������������
b.��������HOOC��CH2CHClCOOH�Ĺ����л����м����OHC��CH2CHClCHO���ɣ�������м������Լ�������������ͭ����Һ����������Һ����


 �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д� ��������ϵ�д�
��������ϵ�д� ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ñ�����ζ�δ֪Ũ�ȵİ�ˮ��Һ(��ƿ��)ʱ������˵����ȷ����
A. ��ȡһ������İ�ˮ������ͼ��ʾ����![]()
B. �Ӳⶨ�����ȷ�Կ��ǣ�ѡ���̪��ָʾ����ѡ����Ҫ��
C. �ζ�ǰ�ζ��ܵļ��촦�����ݣ����ڵζ���������ʧ����ⶨ��ˮ��Ũ��ƫ��
D. �ζ������У�����ƿ�м�����������ˮ�ᵼ�²ⶨ��Ũ��ƫС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��C60�ķ���Ϊ����ѧ�ṩ����Ҫ���о��������й���C60��˵����ȷ���ǣ� ��
A.C60��һ�����ͻ�����B.C60��Ħ��������720
C.C60��һ�ֻ����D.C60����ʯ����̼��ͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�����Ʊ�����ˮ�ij��÷���,��ͼ��ʾ������װ�ö�������ȡ����ˮ��

��1��ͼI��ʵ������ȡ����ˮ�ij���װ��,����A��������________________������AʱҪ�ӵ�ʯ����,Ŀ����_______________��
��2��ˮ�������Ƿ���ȷ?________(������ȷ����������ȷ��)
��3��ʵ��ʱA�г�������������ˮ��,�����������___________,��������____________��
��4��ͼ��װ��Ҳ��������������ˮ����ȡ(���ȼ��̶�������),��ԭ����ͼI��ȫ��ͬ����װ����ʹ�õIJ������ܽϳ�,��������________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �ⶨHCl��NaOH�кͷ�Ӧ�ķ�Ӧ��ʱ������ʵ���Ӧ����3���¶ȣ���������ʼ�¶ȡ�NaOH��Һ��ʼ�¶Ⱥͷ�Ӧ��ֹ�¶�
B. ��2C(s) + O2(g) = 2CO(g) ��H=��221.0kJ/mol����̼��ȼ����Ϊ110.5 kJ/mol
C. ���ˮ���Ի��H2��O2���÷�Ӧ�Ƿ��ȷ�Ӧ
D. ��֪I����ӦH2(g)+Cl2(g)��2HCl(g) ��H=��akJ/mol��II:![]() ��a��b��c�������㣬��Ͽ�1 mol H-Cl�����������Ϊ2(a+b+c) kJ/mol
��a��b��c�������㣬��Ͽ�1 mol H-Cl�����������Ϊ2(a+b+c) kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������У��������۲�����һ������CO���壬һ�������·������淴Ӧ��Ni(s)+4CO(g)![]() Ni(CO)4(g)����֪�÷�Ӧ��25�桢80��ʱ��ƽ�ⳣ���ֱ�Ϊ5��104��2������˵����ȷ����(�� ��)
Ni(CO)4(g)����֪�÷�Ӧ��25�桢80��ʱ��ƽ�ⳣ���ֱ�Ϊ5��104��2������˵����ȷ����(�� ��)
A. ��������Ni(CO)4(g)�ķ�ӦΪ���ȷ�Ӧ
B. 80��ʱ�����ijʱ��Ni(CO)4(g)��CO(g)Ũ�Ⱦ�Ϊ0.5 mol/L�����ʱv(��)��v(��)
C. ���º�ѹ�£����������ٳ���������Ar������ƽ�⽫�����ƶ�
D. ����ʱ�����������С��ԭ����һ�룬�ﵽ��ƽ��ʱCOŨ�Ƚ�Ҫ��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�������ɺ�������ԭ���ʹ������ ( )
A. Fe2(SO4)3 B. KCl C. FeCl3 D. Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ�Ĺ�ҵԭ�ϣ���ũҵ��ҽҩ�������ͻ�������������ҪӦ�á�
I.��1����ҵ����N2��H2��һ�������ºϳɰ������д�ʩ��ʹ����Ӧ����������ʹƽ��������NH3���������һ���������______��
A.���ͷ�Ӧ�¶� B.ѹ����Ӧ����� C.����N2 D.Һ������NH3
��2����������100m10.2mol/L�İ�ˮ����μ���0.2mol/L�����ᣬ������Һ��pH����Һ��NH4+��NH3��H2O���ʵ���������������������Ĺ�ϵ����ͼ��ʾ������ͼ��ش��������⡣
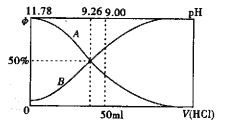
�ٱ�ʾNH3��H2OŨ�ȱ仯��������______(����A������B")��
��NH3��H2O�ĵ��볣��Ϊ_______(��֪1g1.8=0.26)
�۵������������Ϊ50mlʱ����Һ��c(NH4+)-c(NH3��H2O)=____mol/L(�þ�ȷֵ��ʾ)��
II.��֪�����£�Ksp[Al(OH)3]=4.0��10-38����AlCl3��Һ�м���NaHCO3��Һ�������������壬��Ӧ�����ӷ���ʽΪ:________________��������������Һ��pH����Ϊ3������Һ��Al3+Ũ��Ϊ_____mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ,��0.10m/L������BOH�ζ�10.00 ml a mol/L������,��Һ��pH������BOH��Һ���(V)�Ĺ�ϵ��ͼ��ʾ����֪N����Һ�д��ڹ�ϵʽ:c(C1��)=c(B+)+c(BOH)������˵����ȷ����

A. M����Һ�д���c(H+)=c(OH��)+2c(BOH)+c(B+)
B. N��Q������Һ��BOH����ƽ�ⳣ��:N<Q
C. P��BOH����,��ʱ��Һ��c(B+)>c(Cl��)
D. a<0.108
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com