
| A�����ü������ȼƲⶨ��Ӧ��ʱ����ʹ������ĭ����ȱ��µ����á����β�����������н��衢��ͼ����÷�Ӧ��ȡ2-3 �ε�ʵ��ƽ��ֵ���Դﵽ���õ�ʵ��Ч�� |
| B�����ʵ��ܽ��Խ����Һ��Ũ��Խ�ߣ��ܼ��������ٶ�Խ�죬��Һ����ȴ�ٶ�Խ�죬�����ľ����ԽϸС |
| C�����˲����У�������ϻ���;��ֹͣ����ʱ��Ӧע���Ȳ������ӳ����ú�����ƿ����Ƥ�ܣ�Ȼ��ر�ˮ��ͷ���Է����� |
| D��Ϊ��֤���ŵ����ã��������ձ��зֱ�ʢ���������������Һϡ�����Ը��������Һ���ֱ����ʯī���õ����������������Ȼ����װ��K2SO4������Һ����֬��U�����˲��������ձ��У�������ƫת��һ��ʱ�����������Һ��ɫ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ȼҩ�����β�������ҩ���ж������� |
| B��ʹ����ù��ʱ��ֱ�Ӿ���ע����Բ��ý���Ƥ���������� |
| C�����ڴ���ʹ�ð�˾ƥ�ֿ�Ԥ��������û�и����� |
| D����Ƽ������ߵ�Ч�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶�/�� | 25 | T1 | T2 |
| ˮ�����ӻ����� | 1.0��10-14 | �� | 1.0��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �ṹ | ������ֻ����һ��������������ֻ��һ��ȡ��������֧�����˴Ź�������ͼ�����������շ壬�������Ϊ1��2��2��1��1��3 |
| ���� | ����ʹ��ˮ������ѧ��Ӧ����ɫ����NaOH��Һ������ˮ�ⷴӦ���ɾ��о綾�Ĵ������� |
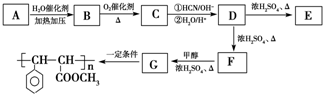
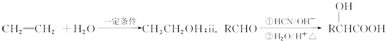
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������Һʱ�ǽ���������Һ���뵽��ˮ�����������ɳ���Ϊֹ |
| B������ƿ���к͵ζ��õ���ƿ������ˮϴ��������ʹ�ã������ʵ���������� |
| C��������������������Ƿ��ж�����̼�����Խ�����ͨ�뵽����̼��������Һ�� |
| D��Ϊȷ�ⶨ������NaOH��Һ��Ӧ���к��ȣ�������ͼ�����ʵ���Ӧ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������Ȳ |
| B���Ҵ�����ϩ |
| C����ϩ�ͻ����� |
| D��������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��2SO2+O2
| ||||
| B��N2��g��+2O2��g��=2NO2��g����H=+67.7kJ/mol | ||||
| C��C��s��+O2��g��=CO2��g����H=+393.5kJ/mol | ||||
D��H2O��l���TH2��g����+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ͼ��ʾ��װ���У���ƿ�г������������a�����ι��ڵ�Һ��b������ƿ�ڣ���������ƿ�������ɼ�f���ձ��е�Һ��b����Ȫ״��������ռ���������ƿ����a��b�ֱ��ǣ�������
����ͼ��ʾ��װ���У���ƿ�г������������a�����ι��ڵ�Һ��b������ƿ�ڣ���������ƿ�������ɼ�f���ձ��е�Һ��b����Ȫ״��������ռ���������ƿ����a��b�ֱ��ǣ�������| a���������壩 | b����Һ�� | |
| A | NO2 | ˮ |
| B | CO2 | ˮ |
| C | Cl2 | ����NaCl��Һ |
| D | NH3 | 1mol?L-1������Һ |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com