
【题目】高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体。下列叙述正确的是
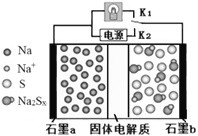
A. 放电时,石墨电极a为正极
B. 放电时,Na+从石墨b向石墨a方向迁移
C. 充电时,b极反应为Na2Sx -2e- = xS+2Na+
D. 可将装置中的固体电解质改成NaCl溶液
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】下列物质的用途错误的是
A. 硅是制造太阳能电池的常用材料 B. 硅是制取水泥的原料
C. 水玻璃可用作木材防火剂 D. 二氧化硅是制造光导纤维的材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A.铁跟氯化铁溶液反应: Fe + 2Fe3+→3Fe2+
B.氨水跟盐酸反应: OH-+ H+→ H2O
C.氢氧化钡跟稀硫酸反应: Ba2++ OH-+ H++ SO42-→ BaSO4↓+ H2O
D.碳酸钙跟盐酸反应: CO32-+2H+→CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.若反应X+Y===M是放热反应,该反应一定不用加热
B.需要加热方能发生的反应一定是吸热反应
C.CO2与CaO化合是放热反应,则CaCO3分解是吸热反应
D.1 mol硫酸与足量氢氧化钠发生中和反应生成水所释放的能量称为中和热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知常温下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.01 molL-1的氨水溶液中滴加相同浓度的CH3COOH溶液,在滴加过程中溶液的pH与所加醋酸的体积关系如图所示。 已知100.4=2.5,下列说法错误的是
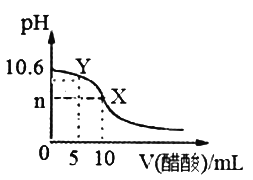
A. n=7
B. 水的电离程度先增大再减小
C. 常温下醋酸的电离常数约是1.67×10-5
D. Y点溶液中c(NH3·H2O)+c(OH-)=c(CH3COO-)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是某兴趣小组通过实验获得的相同体积足量稀硫酸与铁反应的实验数据:
实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | 实验 温度/℃ | 金属消失 的时间/s |
1 | 0.10 | 丝 | 0.7 | 20 | 250 |
2 | 0.10 | 丝 | 1.0 | 20 | 200 |
3 | 0.10 | 粉末 | 1.0 | 20 | 125 |
4 | 0.10 | 粉末 | 1.0 | 30 | 50 |
分析上述数据,回答下列问题:
(1)反应的离子方程式: ;
(2)①实验1、2可得出的结论是,硫酸浓度越 ,反应速率越慢;
②实验2、3可得出的结论是反应物接触面越大,反应速率越 ;
③实验3、4可得出的结论是温度越 ,反应速率越快。
(3)①用铁粉和稀硫酸反应制取H2,实验过程中绘制出生成H2的体积(V)与时间(t)的关系如图所示。 试分析判断OE段、EF段、FG段、GH段反应速率(分别用v (OE)、v (EF)、v (FG)、 (GH)表示)最快时段是 。

A.v (OE) B.v (EF) C.v (FG) D.v (GH)
②1min内反应较慢的原因是: ;
一段时间后反应明显加快的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCN超标的电镀废水可用两段氧化法处理:
①NaCN与NaClO反应,生成NaOCN和NaCl
②NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(K=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)HClO的电子式为___________。
(2)第一次氧化时,溶液的pH应调节为____________(选填“酸性”、“碱性”或“中性”);原因是__________________________________________________。
(3)写出第二次氧化时发生反应的离子方程式。_______________________________________
(4)处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO______g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com