
| n |
| V |
| 1mol |
| 2 |
| ||
| 2L |
| 1mol |
| 2 |
| 1mol |
| 2 |
| 0.45mol |
| 1 |


科目:高中化学 来源: 题型:
| A、限制化学发展,关停化工企业 |
| B、发展新能源,如太阳能、风能等 |
| C、提高原子利用率,发展绿色化学 |
| D、推广微生物发酵技术,以沼气替代液化石油气 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
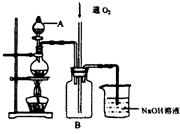 硫酸铜是一种用途广泛的化工原料.将适量稀硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶,得到硫酸铜晶体(装置如图所示).
硫酸铜是一种用途广泛的化工原料.将适量稀硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶,得到硫酸铜晶体(装置如图所示).| 物质 | 开始沉淀时的PH | 完全沉淀时的PH |
| Fe(OH)3 | 1.9 | 3.2 |
| Cu(OH)2 | 4.7 | 6.7 |
| Fe(OH)2 | 6.3 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大力发展火力发电,解决电力紧张问题 |
| B、对杂草、生活垃圾等有机废弃物进行露天焚烧处理 |
| C、汽车安装尾气处理装置,减少大气污染 |
| D、在屋顶安装太阳能热水器为居民提供生活用热水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com