
【题目】I 下列九种物质:①稀硝酸 ②CO ③NH3·H2O ④熔融NaHSO4⑤CaO ⑥Cu ⑦蔗糖⑧Fe2(SO4)3⑨酒精
(1)用序号填空: 属于电解质的是 __________ ;能导电的是_______________ ;
(2)写出④、⑧两种物质在水溶液中的电离方程式:
④______________________________;⑧__________________________________________ 。
II (1)画出S2-的结构示意图_______________________。
(2)质量数为A、中子数为N的离子R2+,该离子的核外电子数为____________。
【答案】 ③④⑤⑧ ①④⑥ NaHSO4= Na++ H++SO42— Fe2(SO4)3= 2Fe3++ 3SO42—  A-N-2
A-N-2
【解析】I(1)①稀硝酸属于混合物,不是电解质也不是非电解质,稀硝酸中含有自由移动的离子H+和NO3-,能导电;②CO在水中和熔融状态下均不能导电,属于非电解质;③NH3 ·H2O溶于水中电离出NH4+和OH-,属于电解质,但NH3 ·H2O不导电,NH3 ·H2O只有溶于水中才可以导电;④NaHSO4属于电解质,在熔融态下能导电;⑤CaO属于电解质,固态的CaO不导电,只有在熔融态下才导电;⑥Cu是金属可以导电,但属于单质,故既不是电解质也不是非电解质;⑦蔗糖是有机物分子,属于非电解质,在水中和熔融态下均不导电;⑧Fe2(SO4)3在水溶液中能电离出自由移动的离子,属于电解质,但固态的Fe2(SO4)3不导电;⑨酒精在水中不导电,为非电解质。根据上面分析可知属于电解质的是③④⑤⑧;能导电的是①④⑥。
(2)NaHSO4是电解质,在水中电离的方程式为:NaHSO4= Na++ H++SO42—;Fe2(SO4)3属于电解质,在水中的电离方程式为:Fe2(SO4)3 = 2Fe3+ + 3SO42—。
II(1)S原子的核电荷数为16,硫原子得到两个电子变成最外层8个电子的稳定结构,离子结构示意图为: 。(2)R原子失去2个电子后变成R2+,质子数和中子数均不变,所以R原子的质子数为A-N,故R2+的核外电子数为A-N-2。
。(2)R原子失去2个电子后变成R2+,质子数和中子数均不变,所以R原子的质子数为A-N,故R2+的核外电子数为A-N-2。


科目:高中化学 来源: 题型:
【题目】由二氧化硅制高纯硅的流程如图,下列判断中错误的是( ) 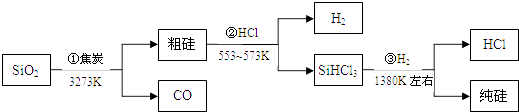
A.①②③均属于氧化还原反应
B.H2和HCl均可循环利用
C.SiO2是一种坚硬难熔的固体
D.SiHCl3摩尔质量为135.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液的PH值不随温度的变化而改变的是( )
A.0.01mol/L的氨水
B.0.01mol/L的NaOH
C.0.01mol/L的CH3COOH
D.0.01mol/L的HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. 从1L 1mol·L-1的NaCl溶液中取出10mL,其浓度仍是1mol·L-1
B. 制成0.5L 10mol·L-1的盐酸,需要氯化氢气体112L(标准状况)
C. 0.5L 2mol·L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023
D. 10g 98%硫酸(密度为1.84g·cm-3)与10mL 18.4mol·L-1硫酸的浓度是不同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能在水溶液中大量共存的离子组是( )
A. Na+、H+、Cl-、CO32-B. Ba2+、H+、SO42-、NO3-
C. Na+、K+、SO42-、CO32-D. Ca2+、Cl-、K+、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某盐酸的物质的量浓度.
(1)标准溶液应盛于(填“A”或“B”)滴定管中. 
(2)若选用酚酞作指示剂,以0.125 0molL﹣1的标准氢氧化钠溶液滴定,如何判断滴定终点
(3)实验数据记录如表,请分析数据并计算,盐酸的物质的量浓度=molL﹣1
滴定次数 | 待测液体体积/mL | 标准碱液 | |
滴定前读数/mL | 滴定后读数/mL | ||
① | 20.0 | 0.40 | 20.41 |
② | 20.0 | 0.10 | 20.60 |
③ | 20.0 | 4.00 | 23.99 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com