
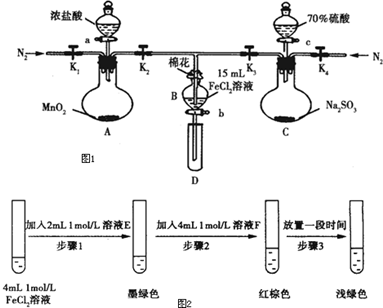
| 过程ⅣB中溶液含有的离子 | 过程ⅥB中溶液含有的离子 | |
| 甲 | 有Fe2+,无Fe3+ | 有SO42- |
| 乙 | 既有Fe3+,又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+,无Fe2+ | 有Fe2+ |
| ||
| ||


科目:高中化学 来源: 题型:
| A、它们的氢化物的稳定性随核电荷数的增加而增强 |
| B、它们单质的氧化性依次减弱 |
| C、它们的原子核外电子层数随核电荷数的增加而增多 |
| D、单质的颜色随核电荷数的增加而加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
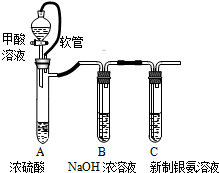 | 已知:银氨溶液制备反应为 Ag++2NH3?H2O═[Ag(NH3)2]++2H2O. 反应结束后试管C底部有黑色沉淀生成,分离出上层清液和底部黑色固体备用. |
查看答案和解析>>
科目:高中化学 来源: 题型:
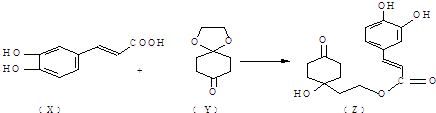
查看答案和解析>>
科目:高中化学 来源: 题型:
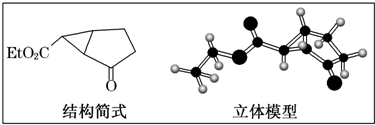
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①③④ |
| C、②③④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 部分短周期元素的原子半径及主要化合价 | ||||||
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
| A、GOH溶液和M(OH)3可以相互反应 |
| B、非金属性:T<Q |
| C、气态氢化物的稳定性:R>T |
| D、L2+与T2-核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲苯的硝化反应生成三硝基甲苯 |
| B、甲苯能使酸性高锰酸钾溶液褪色 |
| C、甲苯燃烧产生带浓烟的火焰 |
| D、1mol甲苯与3mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、流水、风力是一次能源,电力、蒸汽是二次能源 |
| B、普通锌锰电池是一次电池,碱性锌锰电池是二次电池 |
| C、同周期元素形成的简单离子中,原子序数越大的离子半径越小 |
| D、原子核外电子层数越多,原子半径一定越大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com