
【题目】下列实验方法能达到实验目的的是
A. 用淀粉溶液检验溶液中是否存在碘化钾
B. 用分液漏斗分离苯与酒精的混合物
C. 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液
D. 用丁达尔效应区分氢氧化铁胶体和FeCl3溶液
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】能量是国民经济发展的重要基础,天然气是我国目前使用的主要能源。
(1)已知
化学键 | C-H | C=O | O=O | H-O |
E/(KJ/mol) | a | b | c | d |
CH4(g)+2O2(g)=CO2(g)+2H2O(g)的焓变ΔH=______kJ/mol。
(2)燃料电池具有高的发电效率,因而受到重视。下图甲为甲烷燃料电池(电解质溶液为硫酸)该电池的正极反应为_________。
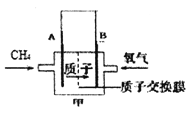
(3)利用上述燃料电池,按下图所示装置进行电解,A、B、C、D均为铂电极,
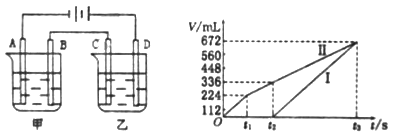
I.甲槽中有200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如上图所示(气体体积已换算成标准状况下的体积),(电解前后溶液的体积变化关系忽略不计)
①原混合溶液中NaCl的物质的量浓度__________mol/L。
②t2时所得溶液的pH=________。
Ⅱ.乙槽中为足量的AgNO3溶液。则阳极反应为__________。t3时电解结束,为了使溶液恢复原样,则可以在反应后的溶液中加入______(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 1 mol NaHSO4熔融或溶于水时电离出的离子总数均为3NA
B. 17 g H2O2含有0.5NA个非极性共价键
C. 在1L0.5mol/LH2SO4溶液中,含有的氧原子数为2NA
D. 标准状况下,22.4 L Cl2溶于水转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用新方案和新工艺处理废旧铅酸蓄电池,可以达到节能减排、防治污染和资源循环利用的目的。一种处理铅酸蓄电池的流程如下:
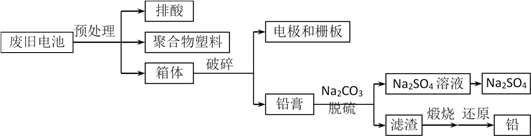
已知:Ksp(PbSO4)=1.6×10-8)和Ksp(PbCO3)=7.4×10-14
(1)写出铅酸蓄电池放电时的总反应____________________________________________;
(2)废旧电池的预处理时需要将电池放电完全,目的是____________________________;
(3)写出铅膏脱硫时的离子方程式____________________________________________。
(4)传统的铅蓄电池的处理工艺是将电池破碎后,洗涤,干燥,直接送入回转炉熔炼。而该工艺使用纯碱脱硫的显著优点是________________________________________。
(5)从Na2SO4溶液中结晶出Na2SO4·10H2O晶体的方法是蒸发浓缩、___________、过滤洗涤,洗涤时用乙醇洗涤晶体,用乙醇而不用水洗涤的原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平。E是具有果香气味的液体。A、B、C、D、E在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
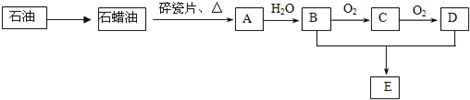
请回答下列问题:
(1)丁烷是由石蜡油获得A的过程中的中间产物之一,它的一种同分异构体中含有三个甲基(![]() ),则这种同分异构体的结构简式是:___________________; D物质中官能团的名称是_______________。
),则这种同分异构体的结构简式是:___________________; D物质中官能团的名称是_______________。
(2)反应B→C的化学方程式为_____________________________。
(3)反应B+D→E的化学方程式为______________________;该反应的速率比较缓慢,实验中为了提高该反应的速率,通常采取的措施有_______________(任写一项)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.碳酸钙与盐酸反应:CO32﹣+H+═H2O+CO2
B.铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2
C.硝酸与氢氧化钡反应:OH﹣+H+═H2O
D.铜片插入硝酸银溶液中: Cu+Ag+=Cu2++Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等量的CO(g)和H2O(g)分别通入到容积为2 L的恒容密闭容器中进行如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),得到下列数据:
CO2(g)+H2(g),得到下列数据:
实验组 | 温度 | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
H2O | CO | H2 | |||
1 | 650 | 2 | 4 | 1.6 | 5 |
2 | 900 | 2 | 4 | 0.9 | t |
①在实验1中,以v(CO2)表示该反应前5分钟的平均反应速率为________; __________;平衡时的压强和反应开始的压强之比为__________。
②在实验2中,t________5(填“大于”“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Se是制光电池的一种原料。电解铜的阳极泥中含有3%-14%的Se元素(Se元素以Se单质和Cu2Se的形式存在),还含有稀有金属及贵金属。从阳极泥中提取Se的流程如下:
![]()
请回答下列向题:
(1)浓硫酸溶解Cu2Se生成CuSO4、SO2、SeO2的化学方程式为__________________。
(2)流程②的目的是_____________________。
(3)流程④的操作名称是_____________________。
(4)SO2与SeO2(g)反应的离子方程式为________________。根据上述提取Se的工艺流程可知,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是_____________。
(5)工业提取Se的流程中,可循环利用的物质是________________。(填化学式)
(6)①称取5.000g电解铜阳极泥样品。以合适方法溶解,配成250.0mL混酸溶液
②移取上述溶液25.00mL于锥形瓶中,加入30.0mL0.0100mol/LKMnO4标准溶液(Se由+4价转化为+6价)。
③反应完全后,用0.05000mol/L(NH4)2Fe(SO4)2标准溶液滴至终点,消耗(NH4)2Fe(SO4)2标准溶液10.00mL。
则电解铜阳极泥样品中Se的质量分数为__________________。若用FeCl2标准溶液代替(NH4)2Fe(SO4)2标准溶液进行滴定,对测定Se的质量分数结果__________(其“偏高”或“偏低”“ 无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造如图(a)所示。回答下列问题:
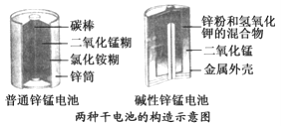
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2===Zn(NH3)2Cl2+2MnOOH,该电池中,负极材料主要是______________,电解质的主要成分是________,正极发生的主要反应是________________________
(2)与普通锌锰电池相比,碱性锌锰电池的优点及其理由是____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com