
| A�� | NaCN��HCN 1��1��ɵ���Һ������ | |
| B�� | 0.1mol•l-1��NaF��NaNO2��NaCN��Һ��pH������ | |
| C�� | ����������Ӧ���ɵó���������ĵ��볣����ֵ | |
| D�� | K��HCN����K��HNO2����K��HF�� |
���� ��ĵ���ƽ�ⳣ��Խ��������Խǿ��ǿ���ܺ������η�Ӧ�������ᣬ����NaCN+HNO2�THCN+NaNO2��NaCN+HF�THCN+NaF��NaNO2+HF�THNO2+NaF֪�����������ǿ��˳����HF��HNO2��HCN����HF��HNO2��HCN��Ӧ�ĵ���ƽ�ⳣ���ֱ��ǣ�7.2��10-4��4.6��10-4��4.9��10-10�����������Խ������������ӵ�ˮ��̶�Խ���Դ˽����⣮
��� �⣺A�������Ϸ�����֪HCN��Ӧ�ĵ���ƽ�ⳣ��Ϊ4.9��10-10����ˮ�ⳣ��Ϊ$\frac{1��1{0}^{-14}}{4.9��1{0}^{-10}}$����֪ˮ��̶Ƚϴ���NaCN��HCN 1��1��ɵ���Һ�ʼ��ԣ���A����
B�����ǿ��˳����HF��HNO2��HCN�����������ε�ˮ�������С˳��ΪNaF��NaNO2��NaCN����B��ȷ��
C������NaCN+HNO2��HCN+NaNO2��NaCN+HF��HCN+NaF���ɵó�������ĵ��볣����ֵ����C��ȷ��
D����ĵ���ƽ�ⳣ��Խ��������Խǿ�����������ǿ��˳����HF��HNO2��HCN������K��HCN����K��HNO2����K��HF������D��ȷ��
��ѡA��
���� ���⿼����������ʵĵ��룬��ȷ���ǿ���������ƽ�ⳣ���Ĺ�ϵ�ǽⱾ��ؼ������ǿ����ȡ���������������Ŀ�ѶȲ���


 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���᳧������豸�����⼣�߰� | |
| B�� | ���죬���������׳������ | |
| C�� | ������ʢװ�����ˮ��������©ˮ | |
| D�� | ����ˮͭ����ͷ�����ܽӿڴ����ֺ��ɫ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
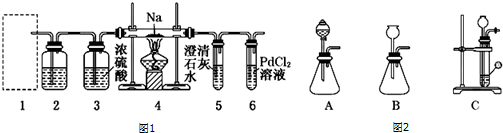
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڡ��������ⸯʴ��ʵ���У����������ͭ˿�������ϲ������ݶ࣬��Χ�ȳ�����ɫ ��������Һ�еμӼ���K3[Fe��CN��6]��Һ�� | |
| B�� | ��Zn-CuϡH2SO4���ɵ�ԭ����У��ú������ZnƬ��CuƬ����Ŀ���ǽ��͵缫֮������裬��ǿ�ŵ�Ч�� | |
| C�� | ��Zn-CuϡH2SO4���ɵ�ԭ����У���Һ�м�������H2O2����Ŀ���ǽ��͵缫�ļ������ã���ߵ�صķŵ�Ч�� | |
| D�� | ������ͭ����ⱥ��ʳ��ˮ��2C1-+2H2O���2OH-+H2��+C12�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���ڿ����о��õ���Ƭ5.0gͶ��ʢ��50mL 0.1mol•L-1������Һ���ձ��У�����Ƭ�����ᷴӦ����������������v��H2���뷴Ӧʱ��t�Ĺ�ϵ��������ͼ��ʾ��������������ʾ���������۴�����ǣ�������
���ڿ����о��õ���Ƭ5.0gͶ��ʢ��50mL 0.1mol•L-1������Һ���ձ��У�����Ƭ�����ᷴӦ����������������v��H2���뷴Ӧʱ��t�Ĺ�ϵ��������ͼ��ʾ��������������ʾ���������۴�����ǣ�������| A�� | O��a�β�������������Ϊ��������������������ϡ���� | |
| B�� | b��c�β����������������ӽϿ����Ҫԭ��֮һ���¶����� | |
| C�� | t=cʱ�̣���Ӧ����ƽ�� | |
| D�� | t��cʱ���������������ʽ��͵���Ҫԭ������Һ��H+Ũ���½� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
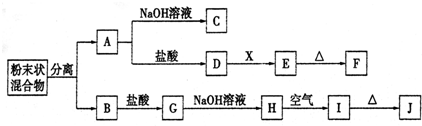
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com