
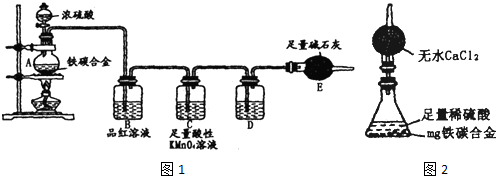
 CO2Ўь+COЎь+H2OУРИЛАыУГХвёц·ґУ¦ІъЙъµДCO»№ФДіЦЦМъµДСх»ЇОпЈ¬ІўЙијЖБЛИзПВНјЛщКѕµДЧ°ЦГЎЈЖдЦРAєНFЦРёчКўУРЕЁH2SO4Ј¬BЦРКўУРТТ¶юЛбЈЁH2C2O4Ј©Ј¬DЦРКўУРNaOHЕЁИЬТєЈ¬EєНIЦРёчКўУРіОЗеКЇ»ТЛ®Ј¬HЦРЧ°УРМъµДСх»ЇОп·ЫД©ЎЈ
CO2Ўь+COЎь+H2OУРИЛАыУГХвёц·ґУ¦ІъЙъµДCO»№ФДіЦЦМъµДСх»ЇОпЈ¬ІўЙијЖБЛИзПВНјЛщКѕµДЧ°ЦГЎЈЖдЦРAєНFЦРёчКўУРЕЁH2SO4Ј¬BЦРКўУРТТ¶юЛбЈЁH2C2O4Ј©Ј¬DЦРКўУРNaOHЕЁИЬТєЈ¬EєНIЦРёчКўУРіОЗеКЇ»ТЛ®Ј¬HЦРЧ°УРМъµДСх»ЇОп·ЫД©ЎЈ

ўс.ЈЁ1Ј©DЧ°ЦГµДЧчУГКЗ________ЎЈ
ЈЁ2Ј©EЧ°ЦГµДЧчУГКЗ________ЎЈ
ЈЁ3Ј©IЧ°ЦГµДЧчУГКЗ________ЎЈ
ўт.јЧН¬С§УГЙПКцЧ°ЦГЈ¬ИЎІ»Н¬ЦКБїµДМъµДСх»ЇОпЅшРРКµСйЎЈЛщµГКµСйКэѕЭИзПВЈє
|
КµСйРтєЕ |
МъµДСх»ЇОпЦКБї/g |
ЙъіЙМъµДЦКБї/g |
|
1 |
4.00 |
2.81 |
|
2 |
8.00 |
7.62 |
|
3 |
10.00 |
7.01 |
|
4 |
12.00 |
8.42 |
|
5 |
14.00 |
9.81 |
|
6 |
16.00 |
12.22 |
|
7 |
18.00 |
12.63 |
|
8 |
20.00 |
14.03 |
ЈЁ1Ј©Из№ыТФyЦб±нКѕЙъіЙМъµДЦКБїЈ¬xЦб±нКѕМъµДСх»ЇОпЦКБїЈ¬ЗлУГЗ¦±КФЪЙПГжЧш±кНјЙПТАґОХТіцПаУ¦µДКµСйКэѕЭµДµгЎЈ

ЈЁ2Ј©ґУЧш±кНјЙПїЙТФїґіцјЧЅшРРµЪ¶юґОКµСйК±Ј¬ЛщµГКэѕЭІ»К®·ЦїЙїїЈ¬№КЙбИҐЎЈЗл·ЦОцФміЙґЛЦЦЅб№ыµДФТтЦчТЄїЙДЬКЗ________»т________ЎЈ
ЈЁ3Ј©ЗлАыУГЙПНј»ШґрЎЈµЪ¶юґОКµСйК±ЙъіЙµДМъµДЦКБїФјОЄ________gЈЁРЎКэµгєу±ЈБфТ»О»Ј©ЎЈ
ЈЁ4Ј©Из№ыБнТ»О»Н¬С§ТТИЎБЛ25 gМъµДСх»ЇОпСщЖ·¶шАґІ»ј°ЧцКµСйЈ¬µ«ёщѕЭЙПКцНјКѕЈ¬їЙТФЗуіцЛщЙъіЙµДМъµДЦШБїОЄ________ЈЁРЎКэµгєу±ЈБфТ»О»Ј©ЎЈЅ«ДгЛщУГ·Ѕ·ЁФЪЙПНјЦР»іцЎЈ
ЈЁ5Ј©Н¬С§±ыїґБЛјЧЎўТТБЅН¬С§ЛщЧцµД·Ѕ·ЁєуИПОЄЈєЦ»ТЄИПХжЅшРРБЅґОКµСйЈ¬ѕНТФ»ШґрЙПКцОКМвЎЈЗлУГјЧН¬С§µДБЅЧйКµСйКэѕЭЈ¬УГКэС§·Ѕ·ЁРґіц±ыН¬С§µД·ЦОц№эіМЎЈ
ЈЁ6Ј©¶ЎН¬С§їґБЛЙПКц·ЦОц№эіМєуЈ¬ИПОЄЦ»ТЄТ»ЧйЧјИ·µДКµСйКэѕЭѕНДЬЅвѕцОКМвЎЈЛыКЗФхСщ·ЦОцµДЈїSi+O2=SiO2
| ЈЁўсЈ©ЈЁ1Ј©іэИҐ»мєПЖшМеЦРµДCO2 ЈЁ2Ј©јмСй»мєПЖшЦРCO2КЗ·сТС±»И«ІїОьКХ
ЈЁ3Ј©КЇ»ТЛ®±д»лЧЗЈ¬ЛµГчЙъіЙБЛCO2Ј¬ґУ¶шЦ¤ГчCO»№ФБЛМъµДСх»ЇОпІўіэИҐCO2 ЈЁўтЈ©ЈЁ1Ј©јыПВНјЎЈ
ЈЁ2Ј©·ґУ¦К±јдМ«¶М ОВ¶ИЖ«µНЎўЈЁ3Ј©5.5ЎА0.2. ЈЁ4Ј©17. 5ЎА0.3 ЈЁ5Ј© yЈЅ0.7x µ±xЈЅ8К±Ј¬y=5.6Ј» xЈЅ25К±Ј¬9ЈЅ17. 5ЎЈ ЈЁ6Ј©Г»УР·ґУ¦ОпТІГ»УРЙъіЙОпµДµгјґФµгЈ¬№эФµгµДЦ±ПЯ·ЅіМЦ»ДЬОЄyЈЅkxЎЈ
|



| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈєФД¶БАнЅв
| ||
| ||
| ||
| ||
| 11m-3b |
| 11m |
| 11m-3b |
| 11m |
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈєФД¶БАнЅв

| ||
| ||
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє

 ЈЁ
ЈЁ »т
»т Ј©
Ј© ЈЁ
ЈЁ »т
»т Ј©
Ј©




Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2010-2011С§ДкєЪБъЅКЎґуЗмКРємёЪЗшМъИЛЦРС§ёЯТ»ЈЁПВЈ©ЖЪЦР»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєЅвґрМв

Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈєФД¶БАнЅв
»ЇС§·ЅіМКЅБ·П°
Т»ЎўУГ»ЇС§·ЅіМКЅ±нКѕПВБРёчЦЦОпЦКµДКµСйКТЦЖ·Ё
1ЎўO2(ИэЦЦ·Ѕ·Ё)Јє
2ЎўH2Јє
3ЎўCl2Јє
4ЎўNH3Јє
5ЎўCO2Јє
6ЎўNOЈє
¶юЎўУГ·ЅіМКЅ±нКѕ№¤ТµЙъІъ№эіМЈЁІОїјСЎРЮўтЈ¬ґш*µДРґАлЧУ·ЅіМКЅЈ¬ЧўТв·ґУ¦МхјюЈ©
1ЎўВȼҵЈЁµзЅв±ҐєНКіСОЛ®Ј©
*Сфј«Јє
*Тхј«Јє
*ЧЬ·ґУ¦Јє
2ЎўЅУґҐ·ЁЦЖБтЛбЈЁБтМъїуОЄФБПЈ©
ўЩ·РМЪВЇЈє Ј»ЖдЦРСх»ЇІъОпОЄЈє
ўЪЅУґҐКТЈє Ј»
V2O5µДЧчУГКЗ Ј¬·ґУ¦ОВ¶ИїШЦЖФЪ400~500ЎжµДФТтКЗ
ўЫОьКХЛюЈє
УГ98%H2SO4ОьКХSO3¶шІ»УГЛ®Ц±ЅУОьКХµДФТтКЗ
ЎЈ
ўЬОІЖшґ¦АнЈє
3ЎўєЈЛ®МбдеЈє
*ўЩВИ»ЇЈє
ўЪґµіц
ўЫОьКХЈє
ўЬЧЄ»ЇЈє
4ЎўєПіЙ°±Јє
ўЩУЙЛ®єНМјєПіЙH2
ўЪєПіЙЛюЈє
5Ўў°±Сх»ЇЦЖПхЛб
ўЩСх»ЇВЇЈє
ўЪОьКХЛюЈє
ўЫЦЖИЎ»Ї·КПхЛбп§:
6ЎўТ±Б¶ВБЈЁ±щѕ§КЇЧчИЫјБЈ©
ўЩјоИЬЈє
ўЪіБµнЈє
ўЫНСЛ®Јє
ўЬµзЅвЈє*Сфј«Јє
*Тхј«Јє
ЧЬ·ґУ¦Јє
7ЎўВБИИ·ЁЦЖМъ
8ЎўУЙИэСх»ЇОЩЦЖОЩ
9Ўў№¤ТµЦЖЖЇ°Ч·Ы
10ЎўЦЖІЈБ§
11Ўў№¤ТµЙъІъКЇ»ТЅ¬
12ЎўБЄєПЦЖјо·ЁЈє
13ЎўёЯґї№иµДЙъІъ
ЎЈ
14ЎўБ¶МъБ¶ёЦ
ўЩ»№ФјБµДЙъіЙЈє
Ј»
ўЪМъµД»№ФЈЁЅ«МъµДСх»ЇОпЈ¬ИзFe2O3»№ФЈ©Јє
ўЫЅ«ЙъМъНСБтИҐБЧЅµµНє¬МјБїјґµГёЦЎЈ
ИэЎўНкіЙПВБР·ґУ¦µД»ЇС§·ЅіМКЅЈЁЧўТвРґ·ґУ¦МхјюЈ©ЎЈ
1ЎўFe + H2O(g)=
2ЎўC+ H2O(g) =
3ЎўCO+ H2O(g) =
4ЎўF2+ H2O=
5ЎўNH3+H2O
6ЎўNO2+ H2O=
7ЎўSO2+ H2O
8ЎўCl2 + H2O=
9ЎўK + H2O=
10ЎўNa2O2+ H2O=
11ЎўCaC2+ H2O=
12ЎўMg3N2+ H2O =
13ЎўAl + NaOH+ H2O=
14ЎўCaCO3+ H2O+ CO2=
15ЎўFe(OH)2+ H2O+ O2=
16ЎўFeCl3+ H2O
17ЎўNH4Cl+H2O
18ЎўNa2CO3+H2O
19ЎўCuSO4+H2OµзЅв
20ЎўNa2S2O3 + HCl =
21ЎўSiO2 + HF=
22ЎўSiO2 + NaOH=
23ЎўNa2SiO3+ HCl=
ЛДЎўРґіцПВБРОпЦК·Ц±рУлNaOHИЬТє·ґУ¦µД»ЇС§·ЅіМКЅЎЈ
1ЎўSi
2ЎўCl2
3ЎўSiO2
4ЎўSO2 (ЧгБї)
5ЎўCO2(РЎБї)
6ЎўH3PO4
7ЎўH2SO4
8ЎўCH3Br
9ЎўAl
10ЎўAl2O3
11ЎўAlCl3
12ЎўAl(OH)3
13ЎўCuSO4
14ЎўNaHCO3
15ЎўCa(HCO3)2(ЧгБї)
16Ўў(NH4)2SO4
ОеЎўРґіцПВБРОпЦККЬИИ»т№вХХµД»ЇС§·ЅіМКЅЎЈ
1ЎўNaHCO3
2ЎўHNO3
3ЎўAgBr
4ЎўH2SO3
5ЎўNH4HCO3
6ЎўCu(OH)2
7ЎўCa(HCO3)2
8ЎўCu2(OH)2CO3
9ЎўH2O2
10ЎўKClO3
11ЎўKMnO4
12ЎўNH4Cl
13ЎўHClO
14ЎўCH4+Cl2
15ЎўH2+Cl2
16ЎўCuO
БщЎўРґіцПВБР·ґУ¦µД»ЇС§·ЅіМКЅєНАлЧУ·ЅіМКЅ
1ЎўSO2К№деЛ®НКЙ«Јє
2ЎўSO2К№ЛбРФёЯГМЛбјШИЬТєНКЙ«Јє
3ЎўЗвСх»ЇМъИЬУЪЗвµвЛбЈє
4ЎўТТ¶юЛбЈЁІЭЛбЈ©К№ЛбРФёЯГМЛбјШИЬТєНКЙ« Јє
5ЎўУГКЇ»ТЛ®УлРЎЛХґтИЬТєЦЖЙХјоЈє
6ЎўБтЛбЗвп§УлЗвСх»Ї±µИЬТє»мєПЈє
7ЎўЖЇ°Ч·ЫИЬТєЦРідИлЧгБїCO2Јє
8ЎўKHSO4УлЗвСх»Ї±µИЬТє»мєПіКЦРРФЈє
9ЎўFe3O4ИЬУЪПЎПхЛбЈє
10ЎўГч·ЇИЬТєЦРјУBa(OH)2ИЬТєЦБіБµнБїЧоґуЈє
ЖЯЎўУГАлЧУ·ЅіМКЅ±нКѕПВБРФЪИЬТєЦРµД·ґУ¦
1ЎўKCl+AgNO3Јє
2ЎўBa(OH)2+H2SO4Јє
3ЎўBaCO3+HClЈє
4ЎўCu(OH)2+HClЈє
5ЎўFe(OH)2+HNO3(ПЎ) Јє
6ЎўFeCl3+KSCNЈє
7ЎўFeBr2+Cl2(ОпЦКµДБїЦ®±ИОЄ1:1)Јє
8ЎўNaBr+Cl2Јє
9ЎўFe+CuCl2Јє
10ЎўZn+AgNO3Јє
11ЎўґїјоЛ®ЅвЈє
12ЎўГч·Їѕ»Л®Јє
13ЎўНєНПЎПхЛбЈє
14ЎўЕдЦЖТш°±ИЬТєЈє
15ЎўNa2O2Н¶ИлПЎБтЛбЦРЈє
°ЛЎўРґіцПВБРОпЦКФЪїХЖшЦР±дЦКµД»ЇС§·ЅіМКЅ
1ЎўNa2SO3Јє
2ЎўNaOHЈє
3ЎўNOЈє
4ЎўNaЈє
5ЎўNa2O2Јє
6ЎўНЙъРвЈє
7ЎўВИЛ®Јє
8Ўў°ЧБЧЈє
9ЎўПЎБтЛбЛб»ЇµДFeSO4ИЬТє±дЧШ»ЖЙ«
10ЎўОЮЙ«KIИЬТє±дЧШ»ЖЙ«
11ЎўЖЇ°Ч·ЫК§Р§Јє
ѕЕЎўРґіцПВБР·ґУ¦µД»ЇС§·ЅіМКЅ
1Ўў»мєПH2SєНSO2ЙъіЙБтєНЛ®Јє
2ЎўМїјУИИ·ЕИлЕЁБтЛбЦРЈє
3ЎўТТґјґЯ»ЇСх»ЇОЄТТИ©Јє
4ЎўТТИ©УлТш°±ИЬТє·ґУ¦Јє
5ЎўТТИ©УлРВЦЖCu(OH)2јУИИЈє
6ЎўНУлЕЁБтЛб№ІИИЈє
7ЎўСх»ЇБтНЁИлЕЁдеЛ®Јє
8ЎўНУлЕЁПхЛб·ґУ¦Јє
9ЎўДѕМїєНЕЁПхЛб№ІИИЈє
10ЎўFeCl3ИЬТєЦРјУИлKIИЬТєЈє
11ЎўёЯГМЛбјШ№ММеЦРµОИлЕЁСОЛбЈє
12Ўў°±Л®НЁИлЙЩБїSO2Јє
13ЎўЖ«ВБЛбДЖИЬТєЦРјУЧгБїПЎБтЛбЈє
14ЎўNaAlO2ИЬТєЦРідИлЧгБїCO2Јє
15ЎўBa(AlO2)2ИЬТєЦРјУИлБтЛбВБИЬТєЈє
16ЎўЗвСх»ЇСЗМъЛ®ИЬТєФЪїХЖшЦР±дЦКЈє
12ЎўВИ»ЇМъИЬТєИЬЅвНЈє
К®Ўў°ґТЄЗуРґ·ЅіМКЅ
1ЎўРґіцёЯОВМхјюПВ·ўЙъµДЦГ»»·ґУ¦ЛДёцЈє
ўЩ
ўЪ
ўЫ
ўЬ
2ЎўРґіцТ»ёцµгИјМхјюПВµДЦГ»»·ґУ¦Јє
3ЎўРґіцТ»ёцјУИИМхјюПВµДЦГ»»·ґУ¦Јє
4ЎўРґіцТ»ёцУРИэЦЦ·ґУ¦ОпµДЦГ»»·ґУ¦Јє
5ЎўРґіц№¤ТµЙъІъЦРРиТЄёЯОВМхјюµД·ґУ¦ЈЁІ»ЙЩУЪ5ёцЈ©µД»ЇС§·ЅіМКЅЈє
6ЎўКФЙијЖТ»ёцКµСйЈ¬јмСйДіИЬТєЦРґжФЪFe2+Ј¬ЗлФЪПВГжµДєбПЯЙП°ґІЩЧчЛіРтРґіцПаУ¦µДАлЧУ·ЅіМКЅЈє ЎЈ
7ЎўЦОБЖОёЛб№э¶аµДТ©ОпЦРіЈУГAl(OH)3Ј¬ИзєОУГСх»ЇВБЦЖИЎЗвСх»ЇВБЈїТЄЗуЦЖИЎ№эіМЦРЛбјоµДУГБїЅµµЅЧоЙЩЎЈ°ґЙъІъЛіРтРґіцПа№ШµДАлЧУ·ЅіМКЅЈє ЎЈ
8Ўў»ЇС§·ґУ¦ЦРУРµДѕЯУРПаЛЖРФЈ¬УРµД·ґУ¦ѕЯУРМШКвРФЈ¬КФРґіцПВБРПа№Ш»ЇС§·ЅіМКЅЈ¬ІўЛјїјЖдЦРµДФТтЈє
ўЩ Li + O2
Na + O2
ўЪ Mg + CO2
Mg + SO2
ўЫ Na2O2 + CO2
Na2O2 + SO2
KO2 + CO2
ўЬ F2 + H2O
Cl2 + H2O
ўЭ Fe + Cl2
Fe + I2
ўЮ Fe(OH)3 + HCl
Fe(OH)3 + HI
9Ўў°ґТЄЗуРґ»ЇС§·ЅіМКЅ
ўЩјоРФСх»ЇОпУлЛ®·ґУ¦ЈЁѕЩ2АэЈ©
ўЪјоРФСх»ЇОпУлЛб·ґУ¦ЈЁѕЩ2АэЈ©
ўЫЅрКфСх»ЇОﵫІ»КЗјоРФСх»ЇОпµДСх»ЇОпУлЛ®·ґУ¦ЈЁѕЩТ»АэЈ©
ўЬЛбРФСх»ЇОпУлЛ®·ґУ¦ЈЁѕЩ2АэЈ¬ЖдЦРТ»АэОЄЅрКфСх»ЇОпЈ©
ўЭДЬУлЛ®·ґУ¦ЙъіЙЛбЈ¬µ«І»КЗЛбРФСх»ЇОпТІІ»КЗјоРФСх»ЇОпСх»ЇОпУлЛ®·ґУ¦µД»ЇС§·ЅіМКЅЈє
ЎЈ
ўЮБРѕЩІ»ЙЩУЪ5АајИДЬУлЗїЛб·ґУ¦Ј¬УЦДЬУлЗїјо·ґУ¦µДОпЦКЈ¬Іў·Ц±рРґіцЛьГЗУлЛбЈЁHClЈ©ЎўјоЈЁNaOHЈ©·ґУ¦µДАлЧУ·ЅіМКЅЈє
AЎўОпЦК»ЇС§КЅЈє
BЎўОпЦК»ЇС§КЅЈє
CЎўОпЦК»ЇС§КЅЈє
DЎўОпЦК»ЇС§КЅЈє
EЎўОпЦК»ЇС§КЅЈє
FЎўОпЦК»ЇС§КЅЈє
GЎўОпЦК»ЇС§КЅЈє
10ЎўДіЛбРФСх»ЇОпЈ¬ЛьДЬУлДіР©Лб·ґУ¦Ј¬ТІДЬУлјо·ґУ¦Ј¬ЗлРґіцХвСщµДСх»ЇОпТ»ЦЦЈ¬ІўРґіцЛьУлЛб·ґУ¦µД»ЇС§·ЅіМКЅєНУлјо·ґУ¦µДАлЧУ·ЅіМКЅЈє
Сх»ЇОп·ЦЧУКЅЈє
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com