
| A. | 在空气中,金属铝表面迅速氧化形成保护层 | |
| B. | 红热的铁丝与水接触,表面形成蓝黑色的保护层 | |
| C. | 常温下,浓硫酸使铝、铁等金属钝化 | |
| D. | 白铁(镀锌)表面有划伤时,仍然不易生锈 |
分析 如果属于原电池反应,则说明符合原电池的构成条件,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
解答 解:A.铝和空气中氧气反应生成氧化铝,属于化学腐蚀,不属于原电池反应,故A错误;
B.铁和水蒸气反应生成四氧化三铁,属于化学腐蚀,不属于原电池反应,故B错误;
C.浓硫酸具有强氧化性与铝、铁发生反应生成致密氧化膜,常温下能够使铝、铁钝化,属于化学腐蚀,不属于原电池反应,故C错误;
D.Zn、Fe和电解质溶液构成原电池,发生电化学腐蚀,属于原电池反应,故D正确;
故选D.
点评 本题考查原电池判断,明确原电池构成及原电池原理即可解答,知道电化学腐蚀和化学腐蚀的区别,生活中电化学腐蚀较普遍,注意积累.


科目:高中化学 来源: 题型:选择题
| A. | FeS和CuS | B. | FeS | C. | CuS | D. | Al2S3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用图1所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 | |
| B. | 用图2所示装置蒸发CuCl2溶液制得CuCl2晶体 | |
| C. | 用图3所示装置可由自来水制得蒸馏水 | |
| D. | 用图4所示装置从C2H5OH与C2H5COOCCH3的混合物中分离出乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 先出现沉淀而后全部溶解 | |
| B. | 当Al3+和SO42-全部沉淀所得沉淀量最大 | |
| C. | 最后只有BaSO4沉淀 | |
| D. | 最后生成0.1mol Al(OH)3和0.2molBaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{(4b-2c)}{a}$ | B. | $\frac{(2b-c)}{a}$ | C. | $\frac{(4b-4c)}{a}$ | D. | $\frac{(2b-2c)}{a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
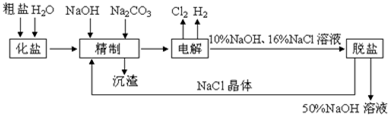
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属性:P<S<Cl | B. | 氢化物稳定性:HF>H2S>H2O | ||
| C. | 碱性:Mg(OH)2>NaOH>Ca(OH)2 | D. | 原子半径:F>Cl>Br>I |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蜡烛的主要成分是烃,属于混合物 | |
| B. | 蚕丝属于纤维素 | |
| C. | “泪”是指石蜡燃烧生成的水 | |
| D. | 蚕丝和石蜡完全燃烧所得的产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
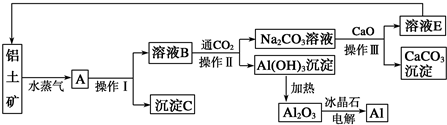
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com