
【题目】用下列装置完成相关实验,不合理的是( )




![]()
A. 用a制备并收集氨气 B. 用b制备并检验乙炔
C. 用c蒸馏海水得到淡水 D. 用d分离Na2CO3溶液与植物油
科目:高中化学 来源: 题型:
【题目】已知固体Na2SO3受热易分解,实验流程和结果如下:
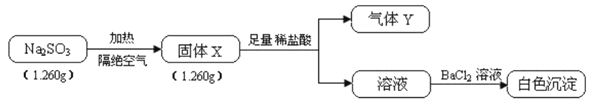
气体Y是一种纯净物,在标准状况下的密度为1.518g·L-1、请回答:
(1)气体Y分子的电子式___,白色沉淀的化学式_______。
(2)该流程中的Na2SO3受热分解的化学方程式__________。
(3)另取固体X试样和Na2SO3混合,加水溶解后与稀盐酸反应,有淡黄色沉淀产生,写出产生淡黄色沉淀的离子方程式____________(不考虑空气的影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实对应的离子方程式或电极反应式书写正确的是( )
A. 用石墨作电极电解CuSO4溶液2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
B. 碳酸钠溶液显碱性:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
C. 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+
D. 在强碱溶液中Fe(OH)3与NaClO反应生成Na2FeO4:3ClO-+2 Fe(OH)3=2FeO42-+3Cl-+H2O+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎。下图是氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是( )

A. a处通入氧气,b处通入氢气
B. P型半导体连接的是电池负极
C. 电池正极电极反应式为O2+2H2O+4e-===4OH-
D. 该装置中只涉及两种形式的能量转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、Mg、Al分别跟稀盐酸充分反应得到相同质量的氢气,其原因是( )
①Fe、Mg、Al的物质的量相等,盐酸足量;
②Fe、Mg、Al的质量比是56∶24∶27,盐酸足量;
③Fe、Mg、Al的质量比是28∶12∶9,盐酸足量;
④Fe、Mg、Al均过量,所用盐酸的浓度和体积都相同。
A. ①② B. ①③ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1 L pH=10的 NaOH溶液中持续通入CO2。通入的CO2的体积(V)与溶液中水电离出的OH- 离子浓度(φ)的关系如下图所示。下列叙述不正确的是( )
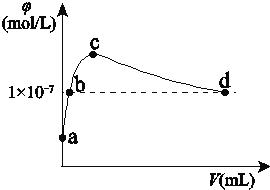
A. a点溶液中:水电离出的c( H+ )=1×10-10mol/L
B. b点溶液中:c( H+ )=c( OH- )
C. c点溶液中:c(OH-) > c(HCO3-)+c( H+ )
D. d点溶液中:c(Na+)=2c(CO32-)+c(HCO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某医药中间体G的一种合成路线如下:
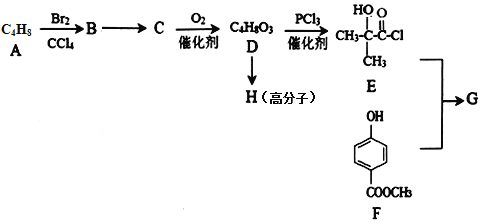
已知:(1)A的核磁共振氢谱有两组峰,且峰面积之比为3∶1;
(2)G的结构简式为:![]() ;
;
(3)![]() 。
。
回答下列问题:
(1)A的名称是_____________;B→C的反应类型是_____________。
(2)G的分子式为___________;G中官能团名称是_____________;1 mol G与NaOH溶液反应最多消耗______ mol NaOH。
(3)H的结构简式为_____________。
(4)D在浓硫酸加热的条件下会生成一种含六元环的化合物,写出该反应的化学方程式_________________________________。
(5)I与F互为同分异构体,则满足下列条件的I的结构有______种(不包括F)。
①苯环上有两个取代基;②遇FeCl3溶液显紫色;③能与NaOH反应。
(6)根据题中所给信息,写出由苯酚,甲苯为原料制备苯甲酸苯酚酯的合成路线(其它无机试剂任选):_________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: Fe2O3+2Al![]() Al2O3+2Fe,回答下列问题:
Al2O3+2Fe,回答下列问题:
(1)在该反应中____元素的化合价升高,该元素的原子_____电子,被____;
(2)在该反应中______元素的化合价降低,该元素的原子________电子,被________。
(3)该反应中,Fe2O3发生了________反应,Al发生了________反应。
(4)_______是氧化剂,_______是还原剂,_______是氧化产物,_______是还原产物。
(5)用单线桥标出电子转移的方向和数目______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 氢化钙固体登山运动员常用的能源提供剂.某兴趣小组长拟选用如下装置制备氢化钙.
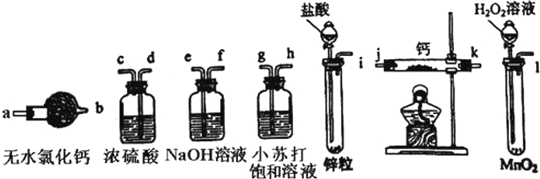
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为__________(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞_________(请按正确的顺序填入下列步骤的标号).
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭分液漏斗活塞 D.停止加热,充分冷却
(3)已知钙与氢化钙固体在外观上相似,现设计一个实验,用化学方法区分钙与氢化钙,请完善以下实验的简要步骤及观察到的现象:取适量氢化钙,在加热条件下与 _________反应,将反应气相产物通过装有_______的容器,观察到容器内固体颜色变化为__________;取钙做类似实验,观察不到类似的反应现象.
II.某化学兴趣小组发现,往CuSO4溶液中加入一定浓度的Na2CO3溶液得到的蓝色沉淀,若加入NaOH溶液则得到浅绿色沉淀。为此,小组同学对蓝色沉淀成份作了如下探究:
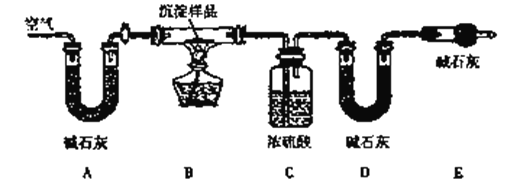
该小组同学利用下列装置通过实验测定其组成
(1)检查装置气密性并装好药品后,点燃酒精灯前应进行的操作是______________。
(2)若沉淀样品的质量为mg。装置C质量增加了ng,则沉淀中CuCO3的质量分数为_____________。
(3)通过查找资料得知,该浅绿色沉淀物可能是溶解度最小的碱式硫酸铜(化学式CuSO4·3Cu(OH)2)。请你设计一个实验,证明浊液中的浅绿色沉淀物中是否含有硫酸根离子的方法__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com