
【题目】下列对于实验I~IV的说法正确的是( )
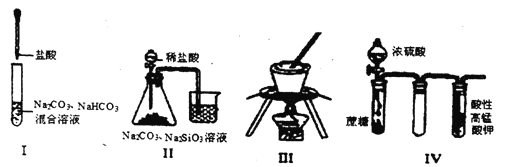
A.实验I:逐滴滴加盐酸时,试管中立即产生大量气泡
B.实验II:可比较氯、碳、硅三种元素的非金属性强弱
C.实验III:从饱和食盐水中提取NaCl晶体
D.装置IV:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去
【答案】D
【解析】A.实验I: 逐滴滴加盐酸时,首先发生反应:Na2CO3+HCl=NaCl+NaHCO3,因此试管中不会立即产生大量气泡,A错误;B.向Na2CO3溶液中加入盐酸,发生反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,证明酸性:HCl>H2CO3,产生的CO2气体通入Na2SiO3溶液中,发生反应:H2O+CO2+ Na2SiO3= Na2CO3+H2SiO3↓,证明酸性H2CO3> H2SiO3,由于盐酸不是Cl元素的最高价态的含氧酸,且生成的CO2中混有氯化氢,因此不能证明元素的非金属性Cl>C>Si,B错误;C.NaCl的溶解度受温度的影响变化较小,要用蒸发结晶的方法获得晶体,蒸发在蒸发皿中进行,而不能在坩埚中进行,C错误;D.浓硫酸有脱水性、强的氧化性,将蔗糖脱水炭化,产生的碳单质被浓硫酸氧化为CO2,硫酸被还原为SO2,SO2有还原性,容易被酸性KMnO4溶液氧化为硫酸而使溶液的紫色褪色,CO2不能反应,从溶液中逸出。因此会看到装置IV:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去,D正确,答案选D。


科目:高中化学 来源: 题型:
【题目】氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是:
![]()
![]()
![]() 据此反应式判断,下列叙述中不正确的是
据此反应式判断,下列叙述中不正确的是
A. 电池放电时,电池负极周围溶液的PH不断增大
B. 电池放电时,正极的电极反应为:![]()
C. 电池充电时,阳极周围溶液的的PH不断减小
D. 电池充电时,阴极的电极反应为:2![]() +2
+2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在pH=1的溶液中能大量共存的离子组合是( )
A.Ba2+、Na+、CO32﹣、SO42﹣
B.Mg2+、Cl﹣、Na+、SO42﹣
C.K+、Cl﹣、HCO3﹣、NO3﹣
D.K+、Na+、Fe2+、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作和数据记录都正确的是
A. 用25 mL碱式滴定管量取高锰酸钾溶液,体积为16.60 mL
B. 用标准NaOH溶液滴定未知浓度盐酸,用去NaOH溶液20.50 mL
C. 用10 mL量筒量取8.25 mL盐酸
D. 用pH试纸测得某溶液pH为3.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物X由Na2O、Fe2O3、Cu、SiO2中的一种或几种物质组成。某兴趣小组以两种途径分别对X进行如下实验探究。

下列有关说法不正确的是( )
A.无法判断混合物中是否含有Na2O
B.由II可知X中一定存在SiO2
C.1.92g 固体成分为Cu
D.15.6g混合物X中m(Fe2O3):m(Cu)=1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Na2S溶液中下列关系不正确
A.c(Na+)=2c(S2-)+2c(HS-)+2c(H2S)
B.c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)
C.c(Na+)>c(S2-)>c(OH-)>c(HS-)
D.c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有单双键交替长链(如…一CH=CH—CH=CH—CH=CH一…)的高分子有可能成为导电塑料。2000年诺贝尔化学奖即授予开辟此领域的3位科学家。下列高分子中,可能成为导电塑料的是( )
A.聚乙烯 B.聚氯乙烯 C.聚1,3-丁二烯 D.聚乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下若要使NH4Cl溶液中c(NH4+)/c(Cl-)比值增大,可采取的方法是
A.加少量水 B.加少量NaOH固体
C.加少量浓氨水 D.通入少量HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
则下列说法正确的是
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H1-△H2=△H3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取降温措施
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com