
【题目】能源是人类生存和发展的重要支柱,化学在能源的开发与利用方面起着十分重要的作用。某学习小组按如下图所示装置探究化学能与电能的相互转化:
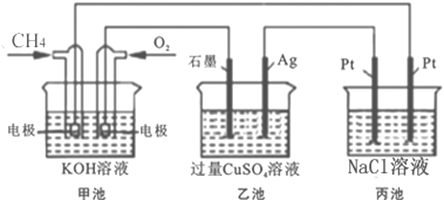
(1)甲池是_________装置,通入O2气体的电极上的反应式为______________。乙池中SO42-移向_____电极(填“石墨”或“Ag”)。
(2) 当甲池消耗标况下33.6L O2时,电解质KOH的物质的量变化_____mol,乙池若要恢复电解前的状态则需要加入__________(填所加物质的质量及化学式)。
(3) 丙池中发生的电解反应的离子方程式为______________。
【答案】原电池(或化学能转化为电能) O2 + 4e- +2H2O===4OH- 石墨 1.5 240gCuO(或372gCuCO3) 2Cl-+2H2O ![]() Cl2↑ + H2↑ + 2OH-
Cl2↑ + H2↑ + 2OH-
【解析】
(1)甲装置为燃料电池,O2在正极上得电子,碱性条件下生成氢氧根离子;乙池为电解池,阴离子移向阳极;
(2)甲装置为燃料,电池总反应为CH4+2O2+2OH-═CO32-+3H2O,据此计算电解质KOH的物质的量变化;乙中为电解硫酸铜溶液,根据电解的产物分析,根据“析出什么元素加入什么元素”的原则确定加入的物质;
(3)丙池为惰性电极电解氯化钠溶液生成氢气、氯气和氢氧化钠,据此书写电解反应的离子方程式。
(1)由图可看出甲图为燃料电池装置,是原电池(或化学能转化为电能);通入氧气的电极为正极,其电极反应式为:O2 + 4e- +2H2O===4OH-;乙图和丙图为电解池,与电池的正极相连的石墨为阳极,与电池的负极相连的Ag电极为阴极,则乙池中SO42- 移向石墨极(阳极),故答案为:原电池(或化学能转化为电能);O2 + 4e- +2H2O===4OH-;石墨;
(2)原电池正极反应式为:2O2+8e-+4H2O=8OH-,总反应为:CH4 +2O2+ 2OH-=CO32-+ 3H2O,当甲池消耗标况下33.6L(1.5mol)O2时,则消耗1.5mol KOH,转移6mol电子,则乙池生成3molCu和1.5molO2,根据原子守恒,若要恢复电解前的状态则需要加入氧化铜:3mol×80g/mol=240g,或碳酸铜:3mol×124g/mol=372g,故答案为:1.5;240gCuO(或372gCuCO3);
(3)丙池中惰性电极电解氯化钠溶液,电解反应的离子方程式为2Cl-+2H2O ![]() Cl2↑ + H2↑ + 2OH-。
Cl2↑ + H2↑ + 2OH-。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列有关性质的比较,不能用元素周期律解释的是
A.酸性:![]()
B.热稳定性:Na2 CO3![]() NaHCO3
NaHCO3
C.与水反应的速率:Na![]() Mg
Mg
D.非金属性:Cl![]() Br
Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,用化学用语回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为___,形成的单质是半导体的是___(填元素名称)。
(2)⑥与⑨形成的化合物的电子式为___,①与②形成的最简单化合物的结构式为___。
(3
(4)气态氢化物最稳定的是___(填化学式),②、③、⑧的原子半径最小是__(填素符号)。
(5)④与⑧形成的化合物的属于___(填“离子化合物”或“共价化合物”),该晶体属于___晶体(填“离子”、“分子”、“原子”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示。下列说法正确的是

A. X难溶于乙醇
B. 酒中的少量丁酸能抑制X的水解
C. 分子式为C4H8O2且官能团与X相同的物质有5种
D. X完全燃烧后生成CO2和H2O的物质的量比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为________,晶体中原子间通过________作用形成面心立方密堆积,其中M原子的配位数为________。
(2)元素Y基态原子的核外电子排布式为________,其同周期元素中,第一电离能最大的是________(写元素符号)。元素Y的含氧酸中,酸性最强的是________(写化学式)
(3)M与Y形成的一种化合物的立方晶胞如图所示。该化合物的化学式为________,已知晶胞参数a=0.542 nm,此晶体的密度为__________g·cm-3。(列式,不要求结果,阿伏加德罗常数为NA)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从海带中提取碘的部分流程如图所示:
![]()

下列说法正确的是
A.完成步骤①需要装置III
B.完成步骤③需要装置I
C.完成步骤⑤需要装置II
D.完成步骤②和④需要装置IV
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为几种化合物的元素组成示意图,以下说法错误的是
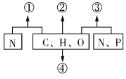
A. 若①为某种具有催化作用的化合物,则其水解产物为氨基酸
B. 若②为脂肪,则其大量积累于皮下和内脏器官周围
C. 若③为蓝藻的遗传物质,则其和蛋白质组成染色体
D. 若④为糖原,则其主要分布在人和动物的肌肉和肝脏中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )
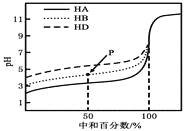
A. 三种酸的电离常数关系:KHA>KHB>KHD
B. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙苯(![]() )、苯乙烯(
)、苯乙烯(![]() )均是重要的有机溶剂和工业原料。
)均是重要的有机溶剂和工业原料。
已知:①![]() (g)+HCl(g)
(g)+HCl(g)![]()
![]() (g) △H1= 54 kJmol1
(g) △H1= 54 kJmol1
②H2(g)+Cl2(g)=2HCl(g) △H2=185 kJmol1
③![]() (g)+Cl2(g)
(g)+Cl2(g)![]()
![]() (g)+HCl(g) △H3=118kJmol1
(g)+HCl(g) △H3=118kJmol1
④相关化学键的键能数据如表所示:
化学键 | CH | CC | C=C | CCl | HCl |
键能/(kJmol1) | 412 | 348 | x | 341 | 432 |
请回答:
(1)x=___;
(2)![]() (g)+H2(g)
(g)+H2(g)![]() (g) △H4
(g) △H4
①△H4=___。
②上述反应中,![]() 的平衡转化率α与温度(T)和压强(P)的关系如图所示。则:
的平衡转化率α与温度(T)和压强(P)的关系如图所示。则:

I.A、B两点的平衡常数:K(A)___K(B)(填“大于”、“小于”或“等于”)。
II.A、B两点的正反应速率:v(A)___v(B)(填“大于”、“小于”或“等于”)。
(3)工业中用乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)。向体积为VL的恒容容器中充入amol乙苯,压强为1×106Pa,在600℃时,平衡体系中苯乙烯的物质的量分数为25%,则:
①乙苯的平衡转化率为___;
②此温度下乙苯催化脱氢的方法制取苯乙烯的平衡常数Kp=___Pa;
③实际生产的反应在常压下进行,且向乙苯蒸气中掺入水蒸气,利用热力学数据计算得到温度和投料比对乙苯转化率的影响可用图表示。[M=n(H2O)/n(乙苯]

a.图中投料比(M1、M2、M3)的大小顺序为___;
b.随着反应的进行,催化剂上的少量积炭使其活性减弱,水蒸气有助于恢复催化剂的活性,原因是___(用化学方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com