
| A. | 0.05mol | B. | 0.1mol | C. | 0.2mol | D. | 0.04mol |
分析 发生Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O,有0.2mol硝酸被还原时,得到电子为0.2mol×(5-4)=0.2mol,Cu失去电子,结合电子守恒计算.
解答 解:发生Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O,有0.2mol硝酸被还原时,得到电子为0.2mol×(5-4)=0.2mol,Cu失去电子,
由电子守恒可知,Cu的物质的量为$\frac{0.2mol}{(2-0)}$=0.1mol,
故选B.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应、元素的化合价变化及电子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol/L | B. | 0.1 mol/L | C. | 0.01 mol/L | D. | 10 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
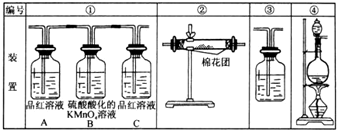 (1)浓硫酸与木炭粉在加热条件下反应的化学方程式是:C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
(1)浓硫酸与木炭粉在加热条件下反应的化学方程式是:C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有气体产生 | B. | 生成白色沉淀 | ||
| C. | 生成无色透明溶液 | D. | 产生气体和白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 组序 成分 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 残留固体成分 | ||||||
| 溶液中的金属离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
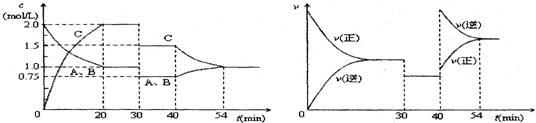
| A. | 30min时减小容积 | |
| B. | 40min时加入催化剂 | |
| C. | 0~20min内A的平均反应速率为0.05mol•L-1•min-1 | |
| D. | 正反应为吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com