
 C60以其完美的球形结构受到科学家的高度重视,从此掀起了球形分子的研究热潮.继C60后,科学家又合成了Si60、N60等球形分子.
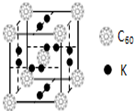
C60以其完美的球形结构受到科学家的高度重视,从此掀起了球形分子的研究热潮.继C60后,科学家又合成了Si60、N60等球形分子.分析 (1)利用均摊法确定K原子和C60分子的个数比;
(2)Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,所以硅原子周围有一个双键和两个单键,双键中有一个π键,每个硅原子只占有$\frac{1}{2}$个π键;
(3)结构相似的分子晶体熔点与其相对分子质量成正比,破坏分子需要断开化学键,元素的化学键的稳定性与元素的电负性成正比
解答 解:(1)根据均摊法可知,该晶胞中C60个数=1+8×$\frac{1}{8}$=2,6×2×$\frac{1}{2}$=6,所以K原子和C60分子的个数比为6:2=3:1,故答案为:3:1;
(2)Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,所以硅原子周围有一个双键和两个单键,双键中有一个π键,每个硅原子只占有$\frac{1}{2}$个π键,所以Si60分子中π键的数目为60×$\frac{1}{2}$=30,
故答案为:30;
(3)Si60、N60、C60都是结构相似的分子晶体,分子晶体的熔点与其相对分子质量成正比,相对分子质量越大,分子间作用力越强,熔化所需能量越多,所以熔点Si60>N60>C60,破坏分子需要断开化学键,元素的电负性越大,其形成的化学键越稳定,断键需要的能量越多,所以破坏分子需要的能量顺序为:N60>C60>Si60,
故答案为:Si60>N60>C60;N60>C60>Si60.
点评 本题考查核外电子排布式的书写、氢键、化学式的确定等知识点,明确影响分子晶体中熔点、化学键大小的因素,为学习难点.


科目:高中化学 来源: 题型:解答题
 化学在能源开发与利用中起着十分重要的作用.
化学在能源开发与利用中起着十分重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 我国前科学院院长卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素(H2NCONH2)和H2O2形成加合物H2NCONH2•H2O2,不但使H2O2稳定下来,而且结构也没有发生改变,得到了可供做衍射实验的单晶体,经测定H2O2结构如图所示,结合以上信息,下列说法不正确的是( )
我国前科学院院长卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素(H2NCONH2)和H2O2形成加合物H2NCONH2•H2O2,不但使H2O2稳定下来,而且结构也没有发生改变,得到了可供做衍射实验的单晶体,经测定H2O2结构如图所示,结合以上信息,下列说法不正确的是( )| A. | 任何分子式中的“•”都表示氢键 | |
| B. | H2O2是极性分子,其结构简式为HO-OH | |
| C. | H2O2既有氧化性又有还原性 | |
| D. | H2NCONH2与H2O2是通过氢键结合的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
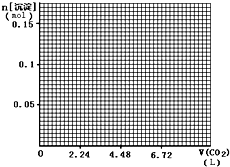 (1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:
(1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:| 溶质 | CH3CO ONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二次电池在充电时,电池的负极要与外接电源的负极相连 | |
| B. | 用惰性电极电解硫酸铜溶液一段时间后,加入氢氧化铜可恢复原状 | |
| C. | 化学腐蚀是生活中最常见的一种金属腐蚀 | |
| D. | 燃料电池中的电极材料必须活性不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 己二酸
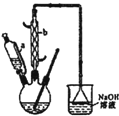
己二酸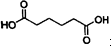 是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位.实验室合成己二酸的反应原理和实验装置示意图如下:
是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位.实验室合成己二酸的反应原理和实验装置示意图如下: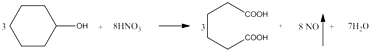
| 物质 | 密度(g/cm3) | 熔点 | 沸点 | 溶解性 | 相对分子质量 |
| 环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 | 100 |
| 己二酸 | 1.360/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 | 146 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com