
下列化学用语或模型表达正确的是
A.乙醇的球棍模型为:
B.次氯酸的结构式为:H一C1一O
C.淀粉的结构简式为:[C6H12O6]n
D.乙烯的电子式为: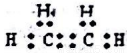
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源:2016届宁夏石嘴山三中高三下四模理综化学试卷(解析版) 题型:填空题
甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
反应 过程 | 化学方程式 | 焓变△H (kJ/mol) | 正反应活化能Ea (kJ/mol) |
甲烷 氧化[ | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | -802.6 | 125.6 |
CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | 172.5 | |
蒸汽 重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 | 240.1 |
CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 | 243.9 |
回答下列问题:
(1)反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H= kJ/mol。
(2)在初始阶段,甲烷蒸汽重整的反应速率 甲烷氧化的反应速率(填大于、小于或等于)。
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应CH4(g)+H2O(g) CO(g)+3H2(g)KP的表达式为 ;随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
CO(g)+3H2(g)KP的表达式为 ;随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量角度分析,甲烷自热重整方法的先进之处在于 。
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:

①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是 。
A.600℃,0.9Mpa B.700℃,0.9Mpa C.800℃,1.5Mpa D.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
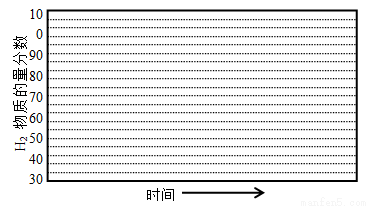
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是 。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三下学期冲刺模拟理综化学A卷(解析版) 题型:选择题
常温下,向10mL 0.1 mol·L-1的HR溶液中逐滴滴入0.1 mol·L-1的氨水,所得溶液pH及导电性变化如图。下列分析不正确的是
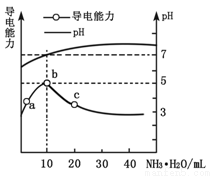
A.b点溶液pH=5,此时酸碱恰好中和
B.a~b点导电能力增强,说明HR为弱酸
C.c点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+)
D.b~c任意点溶液均有c(H+)·c(OH-)=KW=1.0×10-14
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:填空题
己知X、Y、Z、Q、R是原子序数依次增大的短周期元素,X和Q位于同主族,Y、Z、R在元素周期表中的相对位置如图所示,其中Q与R属于同周期.且R的单质常温下是一种黄绿色气体,X2Z2分子和R-离子具有相同的电子数,请回答:
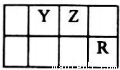
(1)Y元素位于周期表中的第__________族,
(2)化合物Q2Z2中含有的化学键类型有__________。
(3)用电子式表示化合物QR的形成过程:__________。
(4)Y2X4与AgNO3溶液反应可生成Ag、Y2和硝酸,写出该反应的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:选择题
下列三种有机物:①苯酚,②花生油,③木糖醇[CH2OH(CHOH)3CH2OH],它们在常温下的水溶性大小顺序正确的是:
A.①>②>③ B.③>①>② C.③>②>① D.②>①>③
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,高铁酸盐在碱性环境中比酸性环境中相对稳定。工业上用湿法制备高铁酸钾的基本流程如下图所示:
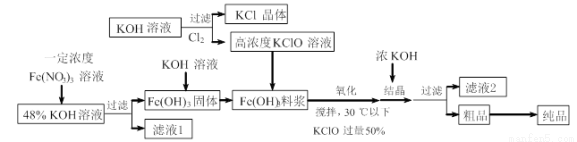
下列有关说法不正确的是
A.控制反应温度30℃以下的原因是防止生成的K2FeO4发生分解
B.结晶过程中加入浓KOH溶液其作用是增大K+浓度,促进K2FeO4晶体析出
C.滤液2中阳离子可通过焰色反应检验确定
D.湿法制备高铁酸钾,也可以在Fe(OH)3料浆中直接通入足量氯气
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中文科化学试卷(解析版) 题型:填空题
本题为《化学与生活(选修1)》选做题
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是 ;
②人体内最重要的供能物质是 ;
③具有解热镇痛作用,用于治疗感冒的是 ;
④对支气管哮喘症有明显疗效的是 。
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是 ;
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为 ;
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的 。
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是 ;
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是 ;
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是 。
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期中化学试卷(解析版) 题型:选择题
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强。下列说法错误的是
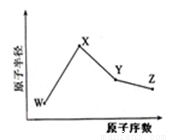
A.对应简单离子半径X<W
B.对应气态氢化物的稳定性Y<Z
C.化合物XZW既含离子键又含共价键
D.Z或X的最高价氧化物对应的水化物均能与Y的氧化物反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com