
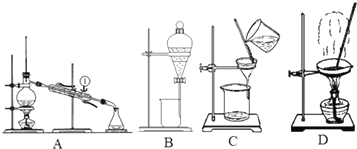
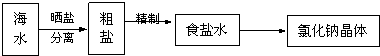
���� ��1�����Ȼ�����Һ�еõ��Ȼ��ع��壬Ӧ�������ķ�������ȥ����ˮ�е�Cl-��������ȡ����ˮ����������ķ�����
��2�������л��ܼ��е��ܽ�Ƚϴ�����ȡ��Һ�ķ������룻
��3�����������Ľṹ�ص����;��ȷ�����������ƣ�װ��B�ڷ�ҺʱΪʹҺ��˳�����£�Ӧʹ��Һ©����ѹǿ�������ѹ��ȣ�
��4�������к�Ca2+��Mg2+��Fe3+��SO42-�����ʣ��ᴿ�����У��ȼ�ˮ�ܽ⣬Ȼ�������ת��Ϊ�����������ȥ����Ca2+��CO32-����Mg2+��Fe3+��OH-����SO42-��Ba2+��Ҫע������ʵ�˳��ӵ��Լ�����ܰ�ǰ���ȼӵĹ����Լ�������
��� �⣺��1���Ȼ�����Һ�еõ��Ȼ��ع��壬Ӧ�������ķ�������ȥ����ˮ�е�Cl-��������ȡ����ˮ����������ķ�����
�ʴ�Ϊ��D��A��
��2�������л��ܼ��е��ܽ�Ƚϴ�����ȡ����Һ�ķ������룬ѡ��װ��B��
�ʴ�Ϊ��B����ȡ����Һ��
��3��װ��A�Тٵ������������ܣ�����ʱ��Ӧ���¶˽�ˮ����ʹ��ˮ���������ܣ��Ա���������
װ��B�ڷ�ҺʱΪʹҺ��˳�����£�Ӧʹ��Һ©����ѹǿ�������ѹ��ȣ��������ΪӦ�Ƚ���Һ©���ϵĻ������º��ٴ������ų�Һ�����ʹ��Һ©�������ϵİ��۶���Һ©�����ϵ�С���ٴ������ų�Һ�壬
�ʴ�Ϊ�������ܣ��¿ڽ�ˮ��Ӧ�Ƚ���Һ©���ϵĻ������º��ٴ������ų�Һ�����ʹ��Һ©�������ϵİ��۶���Һ©�����ϵ�С���ٴ������ų�Һ�壻
��4������1����ȥ�����еĿ��������ʣ�Mg2+��Ca2+��Fe3+��SO42-ʱ���ȼ�ˮ�ܽ⣬���Լ������NaOH��ȥ��þ���Ӻ������ӣ���Mg2++2OH-=Mg��OH��2����Fe3++3OH-�TFe��OH��3�����������BaCl2��ȥ����������ӣ���SO42-+Ba2+=BaSO4�����������Na2CO3��ȥ�������ӵĶ���ı����ӣ���Ca2++CO32-=CaCO3��̼���Ʊ�������Ȼ���֮���������ƺ��Ȼ������Եߵ������˳��Ȼ����ˣ���������Һ��pH����7���������ɣ�������˳���Ǣݢۢڢ٢ޢܢ�ݢڢۢ٢ޢܢߣ�
�ʴ�Ϊ��ad��
����2������ܽ���Һ��pH����7��������������������Ʒ����кͷ�Ӧ����̼���Ʒ�Ӧ���ɶ�����̼��ˮ�Ͷ�����̼����Ӧ�����ӷ���ʽ�ֱ�ΪH++OH-=H2O��2H++CO32-=H2O+CO2����
�ʴ�Ϊ��H++OH-=H2O��2H++CO32-=H2O+CO2����
����3���ɺ�ˮ���Ȼ��ƾ����ʵ�������Ҫ�õ������ķ�����Ϊ��ȥ���ʣ�Ӧ���ˣ���Ҫװ����CD��
�ʴ�Ϊ��CD��
���� ���⿼����������ᴿ����ˮ��Դ���ã�Ϊ��Ƶ���㣬�������ʵ����ʡ����ʲ��켰�������뷽��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/s | 0 | t1 | t2 | t3 | t4 |
| n��SO3��/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
| A�� | ��Ӧ��ǰt1s��ƽ������v��O2��=0.4/t1mol•L-1•s-1 | |
| B�� | ���������������䣬���ѹ����1.0L��ƽ�ⳣ�������� | |
| C�� | �����¶Ȳ��䣬����������ٳ���0.3 molSO2��0.1molO2��0.2molSO3�����ʱV����V�� | |
| D�� | ��ͬ�¶��£���ʼʱ�������г���4mol SO3���ﵽƽ��ʱ��SO3��ת���ʴ���10% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MnO2�ǻ�ԭ�� | B�� | HCl������ | ||
| C�� | MnO2����������Ӧ | D�� | ÿ��Ӧ4molHClת��4mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2CO3��Na2O2 | B�� | Na2CO3 | ||
| C�� | NaOH��Na2CO3 | D�� | Na2O2��NaOH��Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
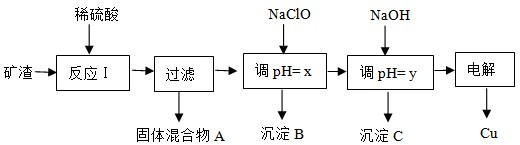
| ���� | Cu��OH��2 | Al��OH��3 | Fe��OH��3 | Fe��OH��2 |
| ��ʼ����pH | 5.4 | 4.0 | 2.2 | 5.8 |
| �������pH | 6.7 | 5.2 | 3.2 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
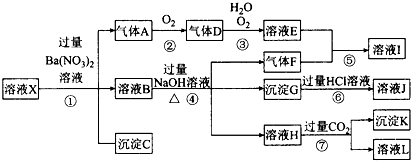
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���ᴿ���� | ���� | �����Լ�����Ҫ�������� |
| A | ���� | ��ϩ | ����KMnO4��Һ��ϴ�� |
| B | MgCl2��Һ | FeCl3 | MgO������ |
| C | HCl���� | Cl2 | ����ʳ��ˮ��ϴ�� |
| D | �Ҵ� | ˮ | ��ʯ�ң����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �þƾ���ȡ��ˮ�еĵ� | |
| B�� | ��������ƽ��ȡ5.20g�Ȼ��� | |
| C�� | ��Һ����ʱ���Ƚ���Һ©�����²�Һ����¿ڷų����ٽ��ϲ�Һ����Ͽڵ��� | |
| D�� | ��������ʱ��Ӧʹ������е�ˮ����ȫ���ɺ���ֹͣ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com