
【题目】Ⅰ.现有下列4种重要的有机物:
①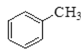 ②
②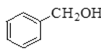 ③
③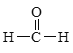 ④
④![]()
请回答:
(1)能与苯酚缩合成高分子化合物的是__________。(填序号)。
(2)能使酸性高锰酸钾溶液褪色的是__________。(填序号)。
(3)写出④在一定条件下发生消去反应的化学方程式__________。
Ⅱ.2020年3月22日为第28届世界水日,化学中有很多与水相关的化学知识。
(1)海水会腐蚀铁质海轮外壳,制造海轮时会在船底四周镶嵌_____。(填“锌块”或“铜块”)
(2)自来水厂常用含有Fe3+的净水剂净水,其原理是______。(用离子方程式表示)
(3)自来水常用氯气杀菌消毒,Cl2+H2OHCl+HClO,要增大HClO的浓度,可以加入下列物质中的__________。
A.NaOH B.浓HCl C.CaCO3固体 D.H2O E.SO2
(4)常温下,0.01mol·L-1NaOH溶液,由水电离出的c(OH)=______mol·L-1。
【答案】③ ①②③ ![]() +NaOH
+NaOH![]()
![]() 锌块 Fe3++3H2OFe(OH)3+3H+ C 10-12
锌块 Fe3++3H2OFe(OH)3+3H+ C 10-12
【解析】
①为甲苯,其属于苯的同系物;②为苯甲醇,其属于芳香醇;③为甲醛,其属于饱和一元醛;④属于卤代烃。通常用牺牲阳极的阴极保护法保护船体。用平衡移动原理分析各物质对化学平衡的影响。
I.(1)能与苯酚缩合成高分子化合物的是甲醛,其合成的高分子为酚醛树脂。答案为③。
(2)甲苯分子中,与苯环直接相连的碳原子上有H;苯甲醇分子中,与苯环直接相连的碳原子上有H,且还有羟基;甲醛分子中有醛基。具有以上这些结构特点的有机物,都能使酸性高锰酸钾溶液褪色,因此,能使酸性高锰酸钾溶液褪色的是①②③。
(3)④在强碱的醇溶液中共热可以发生消去反应生成丙烯,该反应的化学方程式为![]() +NaOH
+NaOH![]()
![]() 。
。
Ⅱ.(1)海水会腐蚀铁质海轮外壳,为了防止其受海水的腐蚀,通常要在船体上连接较活泼的金属(比铁活泼),制造海轮时会在船底四周镶嵌锌块。
(2)自来水厂常用含有Fe3+的净水剂净水,其原理是利用Fe3+的水解产物氢氧化铁胶体吸附水中的悬浮杂质,Fe3+水解的离子方程式为Fe3++3H2OFe(OH)3+3H+。
(3)自来水常用氯气杀菌消毒,Cl2+H2OHCl+HClO,要增大HClO的浓度,应设法让化学平衡向正反应方向移动,且不能消耗HClO。
A.NaOH与产物中的两种酸均可发生中和反应,A不合适;
B.浓HCl可以增大溶液中的氢离子浓度和氯离子浓度,使化学平衡向逆反应方向移动,B不合适;
C.CaCO3固体可以与盐酸反应,但其不与次氯酸反应,可以使化学平衡向正反应方向移动,C合适;
D.加入H2O不能增大次氯酸的浓度,D不合适;
E.SO2消耗氯气和次氯酸,不能增大次氯酸的浓度,E不合适。
综上所述,可以加入CaCO3固体,答案为C。
(4)常温下,0.01mol·L-1NaOH溶液,c(OH)=0.01mol·L-1,由水电离出的c(OH)=c(H+)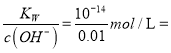 110-12 mol·L-1。
110-12 mol·L-1。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:
【题目】乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a制备,b会发生较多的副反应.回答下列问题:
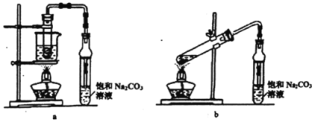
(1)实验时,通常加入过量的乙醇,原因是_____。
(2)饱和Na2CO3溶液的作用是_____。
(3)反应结束后,将盛有饱和Na2CO3溶液的试管中收集到的产品倒入分液漏斗中,_____、_____,然后分液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列叙述正确的是
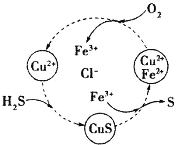
A.在转化过程中化合价不变的元素只有Cu和Cl
B.由图示的转化可得出氧化性的强弱顺序:O2>Cu2+>S
C.在转化过程中能循环利用的物质只有FeCl2
D.反应中当有34gH2S转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O2的质量为16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验的说法不正确的是
A.过滤、萃取、结晶都是依据物质溶解度差异进行的分离提纯
B.可用冷却热饱和溶液的方法除去NaCl中混有的少量KNO3
C.取少量火柴头浸泡液加入硝酸银、稀硝酸和NaNO2,若出现白色沉淀,说明火柴头含氯元素
D.检验海带中碘元素的方法:灼烧→溶解→过滤→氧化→检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是重要的基础有机化工原料。工业中以乙苯催化脱氢来制取苯乙烯:
![]() (g)
(g)![]() (g)+H2(g) H=117.6kJ/mol
(g)+H2(g) H=117.6kJ/mol
已知:上述反应的速率方程为v正=k正P乙苯,v逆=k逆P苯乙烯P氢气,其中k正、k逆分别为正、逆反应速率常数,P为各组分分压。
(1)同时增大乙苯的反应速率和平衡转化率所采取的措施是_______________。
(2)在CO2气氛下,乙苯可催化脱氢制苯乙烯,其过程同时存在如图两种途径:
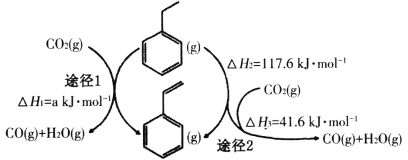
a=______;与掺水蒸汽工艺相比,该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有__________(填序号)。
a.CO2与H2反应,使乙苯脱氢反应的化学平衡右移
b.不用高温水蒸气,可降低能量消耗
c.有利于减少生产过程中可能产生的积炭
d.CO2在反应体系中作催化剂
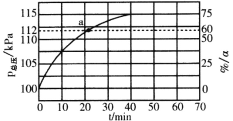
(3)在实际生产中,往反应釜中同时通入乙苯和水蒸气,加入水蒸气稀释剂能提高乙苯转化率的原因是_______________。测得容器总压(P总)和乙苯转化率α随时间变化结果如图所示。平衡时,P(H2O)=_______kPa,平衡常数Kp=____kPa(用平衡分压代替平衡浓度计算);a处的![]() =_________。
=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超分子在生命科学和物理学等领域中具有重要意义。由Mo将2个C60分子、2个p—甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
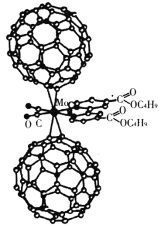
(1)Mo处于第五周期第VIB族,核外电子排布与Cr相似,它的基态价电子排布式是________;核外未成对电子数是________个。
(2)该超分子中配体CO提供孤电子对的原子是________(填元素符号),p—甲酸丁酯吡啶配体中C原子的杂化方式有________。(已知吡啶可看做苯分子中的一个CH原子团被N取代的化合物)
(3)已知:C60分子中存在碳碳单、双键;C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;C60分子只含有五边形和六边形;多面体的顶点数V、面数F及棱边数E遵循欧拉定理:V+F-E=2。则一个C60分子的结构是由_____个五边形和____个六边形组成的球体。用文字简述C60跟F2在一定条件下反应所得的物质的组成:__________________。
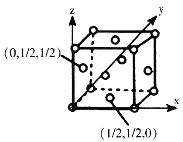
(4)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点的原子坐标均可以为(0,0,0)。钼(Mo)的一种立方晶系的晶体结构中,每个晶胞有2个Mo原子,其中Mo原子坐标是(0,0,0)及(![]() ,
,![]() ,
,![]() )。根据以上信息,推断该晶体的原子堆积方式是_____________。已知该晶体的密度是ρg·cm-3,Mo的摩尔质量是Mg·mol-1,阿伏加德罗常数是NA,晶体中距离最近的Mo原子核之间的距离为_____pm。
)。根据以上信息,推断该晶体的原子堆积方式是_____________。已知该晶体的密度是ρg·cm-3,Mo的摩尔质量是Mg·mol-1,阿伏加德罗常数是NA,晶体中距离最近的Mo原子核之间的距离为_____pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d是原子序数依次增大的短周期主族元素。基态b原子s轨道上的电子总数是基态a原子s轨道上的电子总数的4倍,基态c原子p轨道上的电子数比基态b原子p轨道上的电子数多1,b的原子序数等于d的原子序数的一半,d的最高正价与最低负价的代数和为0。下列说法正确的是( )
A.基态a原子最外层电子排布为![]()
B.最简单氢化物的热稳定性:b>d
C.![]() 中
中![]() 键与
键与![]() 键的数目之比为
键的数目之比为![]()
D.c与其他三种元素形成的二元化合物中,c的化合价一定为-2价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在周期表中,锗和硅位于同主族。四氯化锗(GeCl4)是光导纤维的掺杂剂,其熔点为-49.5℃, 沸点为83.1℃;易水解,对上呼吸道及皮肤有刺激作用。实验室制备四氯化锗的原理是:Ge+2Cl2=GeCl4。某课题组同学拟选择下列装置设计实验制备四氯化锗(部分加热装置和夹持装置省略)。回答下列问题:
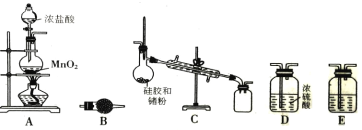
(1)写出A装置中发生反应的化学方程式_______________。
(2)若气体从左到右流动,则装置连接顺序为A、_______________。
(3)C装置中用于冷凝四氯化锗蒸气的仪器名称是_______________,B装置中的试剂是_______________。
(4)E装置中的试剂是_______________,其作用是_______________。
(5)下列有关说法正确的是_______________。
①实验中,先通入氯气,后加热C中烧瓶
②C装置中温度计的温度控制在49℃左右
③观察到D瓶有气泡和液面上有黄绿色气体
④C装置中硅胶的主要作用可能是干燥产品
(6)四氯化锗遇水蒸气产生一种强酸和一种弱酸。实验室用足量NaOH溶液吸收尾气中少量四氯化锗气体,写出该反应的化学方程式:__________________。
(7)实验中消耗m g 纯锗粉制得a g GeCl4,则锗的利用率为_______________(用含 m、a 的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像能说明或反映其对应关系的是( )
|
|
|
|
A | B | C | D |
A.第二周期元素的化合价变化
B.第ⅦA族元素简单阴离子的半径变化
C.向50 mL 0.5mol·L-1NaOH溶液中逐滴加入等浓度盐酸时溶液的pH变化
D.Al与稀硫酸反应产生H2的体积变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com