
| A. | c(Na+)>c(CO32-)>c(HCO3-) | |
| B. | c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| C. | c(Na+)>c(HCO3-)>c(H+)>c(OH-) | |
| D. | c(HCO3-)+2c(CO32-)+c(H2CO3)=1 mol•L-1 |
分析 标准状况下2.24L CO2的物质的量为n(CO2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,n(NaOH)=0.1L×1.5mol/L=0.15mol,则发生反应为:2CO2+3OH-═CO32-+HCO3-+H2O,结合CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-及溶液的电中性原则、物料守恒以及质子守恒解答该题.
解答 解:n(CO2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,n(NaOH)=0.1L×1.5mol/L=0.15mol,则发生:2CO2+3OH-═CO32-+HCO3-+H2O,则溶液中的溶质是等物质的量的碳酸钠和碳酸氢钠,
A.HCO3-水解程度大于其电离程度,CO32-的水解程度大于HCO3-的水解程度,故c(HCO3-)略大于c(CO32-),正确的离子浓度大小为:c(Na+)>c(HCO3-)>c(CO32-),故A错误;
B.根据电荷守恒得:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故B正确;
C.碳酸氢钠和碳酸钠溶液都呈碱性,则c(H+)<c(OH-),正确的离子浓度大小为:c(Na+)>c(HCO3-)>c(OH-)>c(H+),故C错误;
D.根据物料守恒得:c(HCO3-)+c(CO32-)+c(H2CO3)=1mol•L-1,故D错误;
故选B.
点评 本题考查离子浓度大小比较,题目难度中等,明确反应后溶质组成为解本题关键,结合电荷守恒和物料守恒及盐的水解原理分析,试题侧重考查学生的分析、理解能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓、稀硝酸都能使蓝色石蕊试纸最终变为红色 | |
| B. | 硝酸能与Cu反应,只表现氧化性 | |
| C. | 硝酸可与Na2S反应制得H2S气体 | |
| D. | 浓硝酸因分解放出的NO2又溶解于硝酸而呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 页岩气是一种清洁的能源 | |
| B. | 使用页岩气是对化学能的充分利用 | |
| C. | 使用页岩气给农民的生活带来了不便 | |
| D. | 页岩气是我州解决能源的重要途径 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
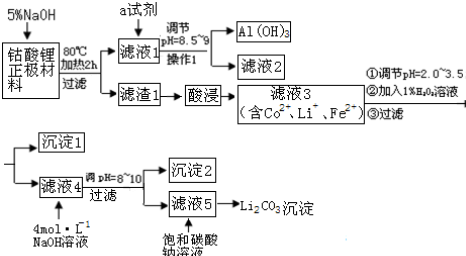
| 金属氢氧化物 | 金属离子浓度 1mol•L-1 | 金属离子浓度 0.1mol•L-1 | 沉淀完全时的pH值 | |
| 分子式 | Ksp | 开始沉淀时的pH | ||
| Fe(OH)2 | 4.87×10-17 | 5.8 | 6.3 | 8.3 |
| Fe(OH)3 | 2.79×10-39 | 1.2 | 1.5 | 2.8 |
| Co(OH)2 | 5.92×10-15 | 6.9 | 7.4 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl、Br2、I2 | B. | NaCl | C. | NaCl、Br2 | D. | NaCl、I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol | B. | 0.75 mol | C. | 0.5 mol | D. | 0.25 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通H2的极是正极,通入O2的极是负极 | |
| B. | 通O2的极是正极,通入H2的极是负极 | |
| C. | 工作一段时间后电解质溶液碱性增强 | |
| D. | 工作时负极区附近碱性不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
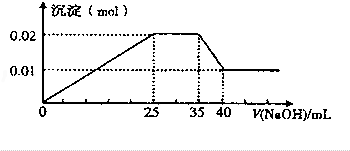 现有一无色溶液含有以下离子(忽略由水电离产生的H+、OH-):NH4+、Mg2+、Al3+、NO3-,取100mL该溶液并逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如图所示,则NO3-的物质的量是( )
现有一无色溶液含有以下离子(忽略由水电离产生的H+、OH-):NH4+、Mg2+、Al3+、NO3-,取100mL该溶液并逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如图所示,则NO3-的物质的量是( )| A. | 0.08mol | B. | 0.07mol | C. | 0.06mol | D. | 0.05mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com