
”¾ĢāÄæ”æŅŃÖŖ²æ·ÖČõĖįµÄµēĄėĘ½ŗā³£ŹżČēĻĀ±ķ£ŗ
ČõĖį | HCOOH | HCN | H2CO3 |
µēĄėĘ½ŗā³£Źż£Ø25”ę£© | K=1.77”Į10-4 | K=5.0”Į10-10 | K1=4.3”Į10-7 K2=5.6”Į10-11 |
ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A. NaCNČÜŅŗÖŠĶØČĖÉŁĮæCO2·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ£ŗCN-+H2O+CO2=HCN+HCO3-
B. µČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄHCOONaŗĶNaCNČÜŅŗÖŠĖłŗ¬ŅõĄė×Ó×ÜŹżĒ°Õß“óÓŚŗóÕß
C. µČĪļÖŹµÄĮæÅØ¶ČµÄNaHCO3ŗĶNa2CO3»ģŗĻČÜŅŗÖŠ£ŗc(Na+)>c(OH-)>c(HCO3-)>c(CO32-)>c(H+)
D. ÖŠŗĶµČĢå»ż”¢µČpHµÄHCOOHČÜŅŗŗĶHCNČÜŅŗĻūŗÄNaOHµÄĪļÖŹµÄĮæĒ°Õߊ”ÓŚŗóÕß
”¾“š°ø”æC
”¾½āĪö”æĻņNaCNČÜŅŗÖŠĶØČėÉŁĮæCO2,ŅņĪŖĖįŠŌ:![]() ,¹Ź·“Ӧɜ³ÉHCNŗĶĢ¼ĖįĒāÄĘ,²»ÄÜÉś³É¶žŃõ»ÆĢ¼,·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ: CN-+H2O+CO2=HCN+HCO3,AÕżČ·£»øł¾ŻµēŗÉŹŲŗć¹ęĀÉ£ŗc(Na+)+c(H+)=c(OH-)+c(CN-)ŗĶc(Na+)+c(H+)=c(OH-)+c(HCOO-)£¬ÓÉÓŚ¼×ĖįµÄĖįŠŌ“óÓŚHCN£¬ĖłŅŌµČĪļÖŹµÄĮæÅØ¶ČµÄHCOONaŗĶNaCNČÜŅŗ£¬NaCNČÜŅŗĖ®½āÄÜĮ¦Ē棬c(OH-)½Ļ“ó£¬c(H+)Ļą¶Ō½ĻŠ”£¬ÓÉÓŚĮ½ČÜŅŗc(Na+)ĻąµČ£¬ĖłŅŌHCOONaČÜŅŗÖŠĖłŗ¬ŅõĄė×Ó×ÜŹż“óÓŚNaCNČÜŅŗĖłŗ¬ŅõĄė×Ó×ÜŹż£¬BÕżČ·£»Ģ¼ĖįÄĘČÜŅŗÖŠĢ¼ĖįøłĄė×ÓĖ®½āÄÜĮ¦“óÓŚĢ¼ĖįĒāÄĘČÜŅŗÖŠĢ¼ĖįĒāøłĄė×ÓĖ®½āÄÜĮ¦£¬ĖłŅŌČÜŅŗÖŠc(HCO3-)>c(CO32-)£»ÓÉÓŚČÜŅŗÖŠµÄc(OH-)ŹĒÓÉc(HCO3-)ŗĶc(CO32-)Ė®½ā²śÉśµÄ£¬ĖłŅŌc(HCO3-)>c(CO32-)> c(OH-)£¬C“ķĪó£»ÓÉÓŚĖįŠŌHCOOH“óÓŚHCN£¬ĖłŅŌµČĢå»ż”¢µČpHµÄHCOOHČÜŅŗŗĶHCNČÜŅŗ£¬HCNČÜŅŗµÄÅØ¶Č½Ļ“ó£¬HCNČÜÖŹµÄĮæ½Ļ“ó£¬ĻūŗÄNaOHµÄĪļÖŹµÄĮæ½Ļ¶ą£¬ ¼“ÖŠŗĶµČĢå»ż”¢µČpHµÄHCOOHČÜŅŗŗĶHCNČÜŅŗĻūŗÄNaOHµÄĪļÖŹµÄĮæĒ°Õߊ”ÓŚŗóÕߣ¬DÕżČ·£»ÕżČ·Ń”ĻīC”£
,¹Ź·“Ӧɜ³ÉHCNŗĶĢ¼ĖįĒāÄĘ,²»ÄÜÉś³É¶žŃõ»ÆĢ¼,·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ: CN-+H2O+CO2=HCN+HCO3,AÕżČ·£»øł¾ŻµēŗÉŹŲŗć¹ęĀÉ£ŗc(Na+)+c(H+)=c(OH-)+c(CN-)ŗĶc(Na+)+c(H+)=c(OH-)+c(HCOO-)£¬ÓÉÓŚ¼×ĖįµÄĖįŠŌ“óÓŚHCN£¬ĖłŅŌµČĪļÖŹµÄĮæÅØ¶ČµÄHCOONaŗĶNaCNČÜŅŗ£¬NaCNČÜŅŗĖ®½āÄÜĮ¦Ē棬c(OH-)½Ļ“ó£¬c(H+)Ļą¶Ō½ĻŠ”£¬ÓÉÓŚĮ½ČÜŅŗc(Na+)ĻąµČ£¬ĖłŅŌHCOONaČÜŅŗÖŠĖłŗ¬ŅõĄė×Ó×ÜŹż“óÓŚNaCNČÜŅŗĖłŗ¬ŅõĄė×Ó×ÜŹż£¬BÕżČ·£»Ģ¼ĖįÄĘČÜŅŗÖŠĢ¼ĖįøłĄė×ÓĖ®½āÄÜĮ¦“óÓŚĢ¼ĖįĒāÄĘČÜŅŗÖŠĢ¼ĖįĒāøłĄė×ÓĖ®½āÄÜĮ¦£¬ĖłŅŌČÜŅŗÖŠc(HCO3-)>c(CO32-)£»ÓÉÓŚČÜŅŗÖŠµÄc(OH-)ŹĒÓÉc(HCO3-)ŗĶc(CO32-)Ė®½ā²śÉśµÄ£¬ĖłŅŌc(HCO3-)>c(CO32-)> c(OH-)£¬C“ķĪó£»ÓÉÓŚĖįŠŌHCOOH“óÓŚHCN£¬ĖłŅŌµČĢå»ż”¢µČpHµÄHCOOHČÜŅŗŗĶHCNČÜŅŗ£¬HCNČÜŅŗµÄÅØ¶Č½Ļ“ó£¬HCNČÜÖŹµÄĮæ½Ļ“ó£¬ĻūŗÄNaOHµÄĪļÖŹµÄĮæ½Ļ¶ą£¬ ¼“ÖŠŗĶµČĢå»ż”¢µČpHµÄHCOOHČÜŅŗŗĶHCNČÜŅŗĻūŗÄNaOHµÄĪļÖŹµÄĮæĒ°Õߊ”ÓŚŗóÕߣ¬DÕżČ·£»ÕżČ·Ń”ĻīC”£


 ĮĮµć¼¤»ī¾«±ąĢįÓÅ100·Ö“óŹŌ¾ķĻµĮŠ“š°ø
ĮĮµć¼¤»ī¾«±ąĢįÓÅ100·Ö“óŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬¼ČÓŠĄė×Ó¼ü£¬ÓÖÓŠ¼«ŠŌ¹²¼Ū¼üµÄŹĒ£Ø £©
A.Na2O2
B.CaCl2
C.KOH
D.H2SO4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÉę¼°»ÆѧѧæĘ¹ŪµćµÄÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ![]()
A. Ī¢Į£¹Ū£ŗ¶žŃõ»ÆĮņŹĒÓÉĮņŌ×ÓŗĶŃõŌ×Ó¹¹³ÉµÄ
B. ×Ŗ»Æ¹Ū£ŗÉżøßĪĀ¶ČæÉŅŌ½«²»±„ŗĶĻõĖį¼ŲČÜŅŗ×Ŗ±äĪŖ±„ŗĶ
C. ŹŲŗć¹Ū£ŗ1gĆ¾Óė1gĻ”ĮņĖį³ä·Ö·“Ó¦ŗóĖłµĆµÄČÜŅŗÖŹĮæĪŖ2g
D. ½į¹¹¹Ū£ŗ½šøÕŹÆŗĶŹÆÄ«ÓÉÓŚ½į¹¹ÖŠĢ¼Ō×ÓµÄÅÅĮŠ·½Ź½²»Ķ¬£¬ŠŌÖŹ“ęŌŚ×ŽĻ“óµÄ²īŅģ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖŌŖĖŲµÄŌ×ÓŠņŹż£¬æÉŅŌĶʶĻŌŖĖŲŌ×ÓµÄ
¢ŁĄė×ÓĖł“ųµēŗÉŹż ¢ŚÖŹ×ÓŹż ¢ŪŗĖµēŗÉŹż ¢ÜŗĖĶāµē×ÓŹż
A.¢Ł¢ŪB.¢Ś¢ŪC.¢Ł¢Ś¢ŪD.¢Ś¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ»śĪļµÄ½į¹¹æÉÓĆ”°¼üĻߏ½”±¼ņ»Æ±ķŹ¾£¬Čē£ŗCH3-CH=CH-CH3æɱķŹ¾ĪŖ![]() £¬ÓŠŅ»ÖÖÓŠ»śĪļX¼üĻߏ½ĪŖ
£¬ÓŠŅ»ÖÖÓŠ»śĪļX¼üĻߏ½ĪŖ![]() ĻĀĮŠ¹ŲÓŚÓŠ»śĪļXµÄŠšŹö“ķĪóµÄŹĒ
ĻĀĮŠ¹ŲÓŚÓŠ»śĪļXµÄŠšŹö“ķĪóµÄŹĒ![]()
A. XµÄ·Ö×ÓŹ½ĪŖC8H8O3
B. ÓŠ»śĪļY×ćXµÄĶ¬·ÖŅģ¹¹Ģ壬ŗ¬ÓŠ±½»·”¢ÄÜÓėNaHC03ČÜŅŗ·“Ó¦”¢ĒŅÓŠČżøöČ”“ś»ł£¬ŌņYµÄ½į¹¹ÓŠ8ÖÖ
C. X·Ö×ÓÖŠµÄĖłÓŠŌ×Ó²»æÉÄÜŌŚĶ¬Ņ»Ę½ĆęÄŚ
D. XÄÜ·¢Éś¼Ó³É·“Ó¦£¬Č”“ś·“Ó¦£¬²¢ÄÜŹ¹äåĖ®”¢ĖįŠŌKMnO4ČÜŅŗĶŹÉ«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČĖ¹¤¹āŗĻ×÷ÓĆÄܹ»½čÖśĢ«ŃōÄÜ£¬ÓĆCO2ŗĶH2OÖʱø»ÆѧŌĮĻ”£ĻĀĶ¼ŹĒĶعżČĖ¹¤¹āŗĻ×÷ÓĆÖʱøHCOOHµÄŌĄķŹ¾ŅāĶ¼£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
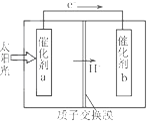
A. øĆ¹ż³ĢŹĒ½«Ģ«ŃōÄÜ×Ŗ»ÆĪŖ»ÆѧÄܵĹż³Ģ
B. “߻ƼĮa±ķĆę·¢ÉśŃõ»Æ·“Ó¦£¬ÓŠO2²śÉś
C. “߻ƼĮaø½½üĖįŠŌ¼õČõ£¬“߻ƼĮbø½½üĖįŠŌŌöĒæ
D. “߻ƼĮb±ķĆęµÄ·“Ó¦ŹĒCO2+2H++2eŅ»=HCOOH
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠĮņĖį¼ŲK2SO4ŗĶĮņĖįĀĮAl2(SO4)3µÄ»ģŗĻČÜŅŗ£¬ŅŃÖŖĘäÖŠAl3£«µÄÅضČĪŖ0.2mol/L,SO42-ÅضČĪŖ0.4mol/LŌņK£«µÄÅضČĪŖ( )
A.0. 1mol/LB.0. 2 mol/LC.0. 3 mol/LD.0.4 mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČÜŅŗÄÜÓėŠæʬ×÷ÓĆ²śÉśH2 £¬ ŌņøĆČÜŅŗÖŠæÉŅŌ“óĮæ¹²“ęµÄĄė×Ó×éŹĒ£Ø £©
A.Na+”¢NO3©”¢K+”¢Fe2+
B.Fe2+”¢Na+”¢SO42©”¢K+
C.K+”¢I©”¢NO3©”¢H+
D.NH4+”¢NO3©”¢Na+”¢HCO3©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijÄųŅ±Į¶³µ¼äÅŷŵÄĘÆĻ“·ĻĖ®ÖŠŗ¬ÓŠŅ»¶ØÅØ¶ČµÄNi2+ŗĶCl-£¬Ķ¼¼×ŹĒĖ«Ä¤ČżŹŅµē³Į»ż·Ø»ŲŹÕ·ĻĖ®ÖŠNi2+µÄŹ¾ŅāĶ¼£¬Ķ¼ŅŅĆčŹöµÄŹĒŹµŃéÖŠŅõ¼«ŅŗpHÓėÄų»ŲŹÕĀŹÖ®¼äµÄ¹ŲĻµ”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A. ½»»»Ä¤bĪŖŅõĄė×Ó½»»»Ä¤
B. Ńō¼«·“Ó¦Ź½ĪŖ2H2O-4e-=O2”ü+4H+
C. Ņõ¼«ŅŗpH= 1Ź±£¬ÄųµÄ»ŲŹÕĀŹµĶÖ÷ŅŖŹĒÓŠ½Ļ¶ąH2Éś³É
D. ÅØĖõŹŅµĆµ½1L 0.5 mol/LŃĪĖįŹ±£¬Ņõ¼«»ŲŹÕµĆµ½11.8 gÄų
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com