在体积为1L的密闭容器中,充入1mol CO
2和3mol H
2,一定条件下发生反应:CO
2(g)+3H
2(g)?CH
3OH(g)+H
2O(g);测得CO
2和CH
3OH(g)的浓度随时间变化如图1所示.该反应过程中的能量变化如图2所示.
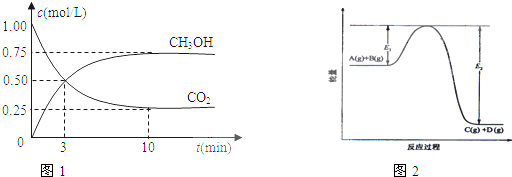
(1)从反应开始到平衡,氢气的平均反应速率v(H
2)=
0.225
0.225
mol/(L?min).
(2)该反应的平衡常数表达式为
K=
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
K=
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
.该条件下的平衡常数K=
5.33
5.33
(可用分数表示),温度升高,K值
减少
减少
(填“增大”“不变”或者“减少”)
(3)如果在达平衡后某一时刻保持温度不变,只改变浓度,使c(CO
2)=1.00mol/L,c(H
2)=0.40mol/L,c(CH
3OH)=c(H
2O)=0.80mol/L,则平衡
b
b
(填写序号).
a.向正反应方向移动 b.向逆反应方向移动 c.不移动 d.无法确定平衡移动方向
(4)下列措施中能使
增大的是
CD
CD
.
A.升高温度 B.充入He(g),使体系压强增大
C.将H
2O(g)从体系中分离 D.再充入1mol CO
2和3mol H
2(5)在反应体系中加入催化剂,E
1和E
2的变化是:E
1减小
减小
,E
2减小
减小
(填“增大”“减小、”“不变”).对反应热是否有影响?
无
无
,原因是
催化剂不能改变反应物的总能量与生成物总能量的差值,即反应热不变
催化剂不能改变反应物的总能量与生成物总能量的差值,即反应热不变
.




 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案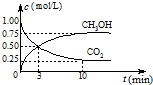
 (2013?珠海模拟)甲醇是一种优质燃料,可制作燃料电池.
(2013?珠海模拟)甲醇是一种优质燃料,可制作燃料电池.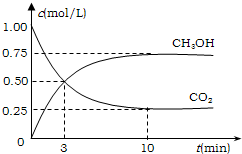 降低大气中CO2的含量及有效地开发利用CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,先进行如下实验,在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.
降低大气中CO2的含量及有效地开发利用CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,先进行如下实验,在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示.