
【题目】除去下列物质中少量杂质所需除杂试剂及方法不正确的是
物质(杂质) | 除杂试剂 | 除杂方法 | |
A | 乙醇(水) | CaO | 蒸馏 |
B | 淀粉溶液(NaCl) | ——— | 渗析 |
C | CO2(HCl) | NaOH溶液 | 洗气 |
D | NaCl溶液(I2) | CCl4 | 萃取分液 |
 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】氧化还原反应在生产生活中有着重要的应用。请按要求写出相应的方程式。
(1)将含SO2的废气通入含Fe2+(催化剂)的溶液中,常温下可使SO2转化为SO2-4,其总反应为2SO2+O2+2H2O=2H2SO4。上述总反应分两步进行,第一步反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,写出第二步反应的离子方程式: 。
(2)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液。若溶液的pH偏高,则碱式硫酸铝产率降低且有气泡产生,用化学方程式表示其原因: 。
(3)ClO2是一种高效安全的杀菌消毒剂。氯化钠电解法生产ClO2工艺原理示意图如下:
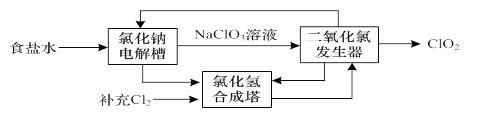
①写出氯化钠电解槽内发生反应的离子方程式: 。
②写出ClO2发生器中的化学方程式,并标出电子转移的方向及数目: 。
③ClO2能将电镀废水中的CN-离子氧化成两种无毒气体,自身被还原成Cl-。写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有NaBr、NaI的溶液中通入过量的Cl2,然后将溶液蒸干,并灼烧固体,最后得到的物质是
A. NaCl B. NaCl和NaBr
C. NaCl和NaI D. NaCl和I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某溶液中由水电离产生的c(H+)等于10-10mol·L-1,该溶液的溶质不可能是( )
A.NaHSO4 B.NaCl
C.HCl D.Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将22.4g铁粉逐渐加入到含HNO3 0.8mol的稀硝酸中,反应生成的气体的物质的量(x)随消耗铁粉的物质的量(y)变化关系中正确的是( )

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片与稀H2SO4反应
B.灼热的炭与CO2反应
C.高温煅烧石灰石
D.甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用3g块状大理石与30mL 3mol/L盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
①再加入30mL 3mol/L盐酸 ②改用30mL 6mol/L盐酸 ③改用3g粉末状大理石 ④适当升高温度.
A. ①②④ B. ②③④ C. ①③④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知丙烷的燃烧热△H= -2215kJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,则放出的热量约为( )
A. 55 kJ B. 220 kJ C. 550 kJ D. 1108 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A. 硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
B. 过氧化钠可用于呼吸面具作为氧气的来源
C. 氧化铁常用作红色油漆和涂料
D. 合金的硬度一般比它的各成分金属的大,熔点一般比它的各成分金属的高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com