
A、B、C、D、E、F六种短周期元素,核电荷数依次增加。只有E为金属,A与E同主族,B与F同主族,B原子最外层电子数是内层电子数的2倍,D最外层有两对成对电子。E+与C3-具有相同的电子层结构。请回答下列问题:
(1)F的价电子排布为______。
B、F形成的化合物晶体类型是_____。
(2)A、B、C、D形成的既有离子键又有共价键的化合物化学式为______。
(3)A、C形成的分子有_____对孤对电子、_____个 键,中心原子杂化方式为______。
键,中心原子杂化方式为______。
(4)稳定性:CA3_____FA4。离子半径:E+_______C3-。(填“>”或“<”
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列说法中,正确的是( )。
A.1 mol Cl2作为氧化剂得到的电子数为NA
B.在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子
C.25 ℃,1.01×105 Pa,64 g SO2中含有的原子数为3 NA
D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列行为中符合安全要求的是
A.进入煤矿井时,用火把照明
B. 实验时,将水倒入浓硫酸配制稀硫
C. 用点燃的火柴在液化气钢瓶口检验是否漏气
D.酸节日期间,在开阔的广场燃放烟花爆竹
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列十种物质:①H2 ②铝 ③CaO ④CO2 ⑤H2SO4
⑥Ba(OH)2 ⑦ 红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质之间可发生离子反应:H++OH-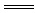 H2O,该离子反应对应
H2O,该离子反应对应
的化学方程式为
(2)⑩在水中的电离方程式为
(3)少量的④通入⑥的溶液中反应的离子方程式为 , 过量的④通入⑥的溶液中
反应的离子方程式为
(4)⑥与过量的碳酸氢钠溶液反应离子方程式:
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,
用双线桥标明电子转移的方向和数目 ,当有5.4g Al发生反应时,转
移电子的数目为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z 的原子序数依次增大,W与Y、X与Z 位于同一主族。W 与X 可形成共价化合物WX2,Y原子的内层电子总数是其最外层电子数的2.5 倍。下列叙述中不正确的是
A.WZ2分子中所有原子最外层都为8 电子结构
B.WX2、ZX2的化学键类型和晶体类型都相同
C.WX2是以极性键结合成的非极性分子
D.原子半径大小顺序为X <W<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
NaNO2像食盐一样有咸味,有很强的毒性,误食亚硝酸钠(NaNO2)会使人中毒。已知亚硝酸钠能发生如下反应:2NaNO2+4HI ===2NO↑+I2+2NaI+2H2O。下列说法正确的是
A.该反应的氧化剂为HI
B.反应产物中能使淀粉变蓝的物质有I2、NaI
C.该反应中氧化剂与还原剂物质的量之比为1:1
D.人误食亚硝酸钠中毒时,可以服用HI溶液解毒
查看答案和解析>>
科目:高中化学 来源: 题型:
利用I2O5可消除CO污染或定量测定CO,反应为:5CO(g)+I2O5(s) 5CO2(g)+I2(s);ΔH1
5CO2(g)+I2(s);ΔH1
(1)已知:2CO(g)+O2(g) 2CO2(g);ΔH2
2CO2(g);ΔH2
2I2(s)+5O2(g) 2I2O5(s);ΔH3
2I2O5(s);ΔH3
则ΔH1=(用含ΔH2和ΔH3的代数式表示)。
(2)不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如下图。请回答:
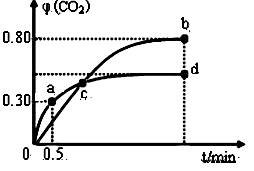
①从反应开始至a点时的反应速率为v(CO)= ,b点时化学平衡常数Kb= 。
②d点时,温度不变,若将容器体积压缩至原来的一半,请在图中补充画出CO2体积分数的变化曲线。
③下列说法正确的是 。(填字母序号)
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的平均相对分子质量相等
C.增加I2O5的投料量有利于提高CO的转化率
D.b点和d点的化学平衡常数:Kb<Kd
(3)将500mL(标准状况)含有CO的某气体样品通过盛有足量I2O5的干燥管,170℃下充分反应,用水—乙醇液充分溶解产物I2,定容到100mL。取25.00mL,用0.0100mol·L-1 Na2S2O3标准溶液滴定,消耗标准溶液20.00mL,则样品气中CO的体积分数为 。(已知:气体样品中其他成分与I2O5不反应;2Na2S2O3+I2=2NaI+Na2S4O6)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列鉴别方法可行的是 ( )
A.用氨水鉴别Al3+、Mg2+和Ag+
B.用Ba(NO3)2溶液鉴别Cl-、SO3-和CO3-
C.用核磁共振氢谱鉴别1溴丙烷和2溴丙烷
D.用KMnO4酸性溶液鉴别CH3CH CHCH2OH和CH3CH2CH2CHO
CHCH2OH和CH3CH2CH2CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
按照题目要求完成下列各小题(每空2分,共20分)
(1)写出下列反应的化学方程式:
①钠与水反应
②Al与氢氧化钠溶液的反应:
③过氧化钠粉末与水的反应:
④Fe与水在高温下反应:
⑤Fe(OH)2在潮湿的空气中转化为Fe(OH) 3:
(2)饱和氯化铁溶液常用于给伤口止血,实验室检验Fe3+的试剂为: ,向盛有氯化铁溶液的试管中滴加该试剂可观察到的实验现象为:
(3)KAl(SO4)2﹒12H2O俗称明矾,常用作净水剂,请用实验方法检验明矾溶液中所含有的主要离子,要求写出检验每种离子的基本操作方法、实验现象及结论。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com