
| A. | 硫在氧气中燃烧 | B. | 硫化氢在氧气中燃烧 | ||
| C. | 铁粉与硫粉混合加热 | D. | 铜在空气中加热 |
分析 A.硫在氧气中燃烧生成二氧化硫;
B.硫化氢在氧气中完全燃烧生成二氧化硫、不完全燃烧生成S;
C.铁粉与硫粉反应生成硫化亚铁;
D.Cu在空气中加热生成氧化铜.
解答 解:A.二氧化硫转化为三氧化硫需要催化剂,硫在氧气中燃烧只能生成二氧化硫,故A不符合;
B.硫化氢在足量的氧气中完全燃烧生成二氧化硫和水,硫化氢与少量的氧气不完全燃烧生成S和水,则通过调节反应物的用量,可以改变反应产物,故B符合;
C.铁粉与硫粉反应生成硫化亚铁,反应物量的多少不会改变反应产物种类,故C不符合;
D.Cu在空气中加热,与氧气反应只生成氧化铜,故D不符合;
故选B.
点评 本题考查了物质的用量或浓度不同导致产物不同,明确物质之间的反应是解本题的关键,难度不大,注意二氧化硫转化为三氧化硫需要催化剂.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:选择题
| A. | 分馏石油获得汽油、煤油和柴油 | |
| B. | 干馏煤获得焦炉煤气、煤焦油和焦炭 | |
| C. | 以煤、石油和天然气为原料生产合成材料 | |
| D. | 从海水中提取溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素、淀粉均属于高分子化合物 | |
| B. | 浓硝酸沾到皮肤上能使皮肤变黄,这是由于浓硝酸和蛋白质发生了颜色反应 | |
| C. | 糖类、油脂、蛋白质都只由C、H、O三种元素组成的 | |
| D. | 利用油脂在碱性条件下的水解,可以制得肥皂和甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
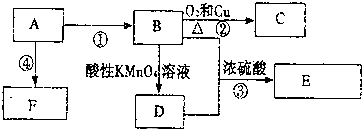
 ,F的结构简式
,F的结构简式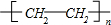 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
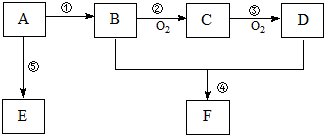
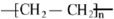 ,B中官能团的名称为羟基.
,B中官能团的名称为羟基. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
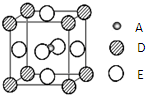 已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大.A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2-离子D2+离子具有相同的、稳定的电子层结构;E的原子序数为28.
已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大.A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2-离子D2+离子具有相同的、稳定的电子层结构;E的原子序数为28.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com