

分析 (1)依据配制一定物质的量浓度溶液一般步骤选择需要仪器,依据配制溶液体积选择容量瓶规格;
(2)依据m=CVM计算需要溶质的质量;
(3)①溶解氢氧化钠应在烧杯中进行;
③移液时,应将玻璃棒下端靠在刻度线以下;
⑤定容时,眼睛应平视刻度线;
(4)依据C=$\frac{n}{V}$进行误差分析,分析不当操作对溶质的物质的量和溶液的体积的影响.
解答 解:(1)配制一定物质的量浓度溶液的步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,用到的仪器有:托盘天平、药匙、玻璃棒、烧杯、容器瓶、胶头滴管;还缺的是:容量瓶,配制450mL 0.100mol•L-1CuSO4溶液,实验室没有450mL容量瓶,应选择500mL规格容量瓶;
故答案为:500ml容量瓶;
(2)实验室用胆矾(CuSO4•5H2O)配制450mL 0.1mol•L-1CuSO4溶液,应选择500ml容量瓶,需要胆矾的质量m=0.1mol•L-1×0.5L×250g/mol=12.5g;
故答案为:12.5;
(3)①溶解氢氧化钠应在烧杯中进行,不能在量筒中进行,故错误;
③移液时,应将玻璃棒下端靠在刻度线以下,图中玻璃棒靠在刻度线以上,故错误;
⑤定容时,眼睛应平视刻度线,图中为仰视操作,导致溶液体积偏大,溶液浓度偏低,故错误;
故选:①③⑤;
(4)①容量瓶使用时未干燥,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故不选;
②定容时俯视刻度线观察液面,导致溶液体积偏小,溶液浓度偏高,故选;
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线,导致溶液体积偏大,溶液浓度偏低,故不选;
④移液时未洗涤烧杯和玻璃棒,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故不选;
⑤胆矾晶体部分失去结晶水,导致秤取的溶质含有硫酸铜的物质的量偏大,溶液浓度偏高,故选;
故选:②⑤.
点评 本题考查了一定物质的量浓度溶液的配制,题目难度不大,明确配制原理及操作步骤是解题关键,注意依据C=$\frac{n}{V}$进行误差分析的方法和技巧.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
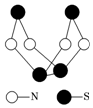 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质的分子式为SN | |
| B. | 该物质的分子中只含共价键 | |
| C. | 该物质具有很高的熔、沸点 | |
| D. | 该物质与化合物S2N2互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 5 | 5 | 55 | 5 |
| 反应后质量/g | 27 | 待测 | 0 | 19 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| B. | 砹单质是一种有色固体,砹化氢很不稳定,砹化银是难溶于水的白色沉淀 | |
| C. | 硫酸锶难溶于水,但易溶于盐酸 | |
| D. | 硒化氢是无色、有毒、比硫化氢稳定的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a% | B. | 2a% | C. | 100%-1.75a% | D. | 100%-0.75a% |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上第一次学段考试化学卷(解析版) 题型:选择题
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为
S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=xkJ•mol-1
已知:碳的燃烧热△H1=akJ•mol-1
S(s)+2K(s)═K2S(s)△H2=bkJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=ckJ•mol-1则x为
A.3a+b-c B.c-3a-b C.a+b-c D.c-a-b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com