
| A. | 4g 氦气中含有的分子数为NA | |
| B. | 常温常压下,22.4LCl2中含有的分子数为NA | |
| C. | 1L1mol/LK2SO4溶液中含有的钾离子数为NA | |
| D. | 1mol钠原子中含有的电子数为NA |
分析 A、氦气为单原子分子;
B、常温常压下气体摩尔体积大于22.4L/mol;
C、求出硫酸钾的物质的量,然后根据1mol硫酸钾中含2mol钾离子来分析;
D、钠原子含11个电子.
解答 解:A、氦气为单原子分子,故氦气的摩尔质量为4g/mol,故4g氦气的物质的量为1mol,则分子个数为NA个,故A正确;
B、常温常压下气体摩尔体积大于22.4L/mol,故22.4L氯气的物质的量小于1mol,则分子个数小于NA个,故B错误;
C、溶液中硫酸钾的物质的量n=CV=1mol/L×1L=1mol,而1mol硫酸钾中含2mol钾离子,即2NA个,故C错误;
D、钠原子含11个电子,故1mol钠原子含11mol电子即11NA个,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 40% | B. | 50% | C. | 80% | D. | 100% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
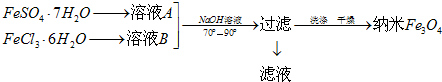
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直接用酒精灯的外焰加热蒸发皿 | |
| B. | 加热过程中不断用玻璃棒搅拌 | |
| C. | 加热到液体全部消失 | |
| D. | 蒸发皿中出现多量晶体、少量液体时,停止加热,利用蒸发皿的余热烘干 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中最多有4种离子 | B. | 若溶液有颜色,则一定没有OH-、I- | ||
| C. | 若溶液呈碱性,则一定含有Na+ | D. | 该溶液不可能溶解单质铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 2 | 1 |
| 5 | 1.2 | |
| 10 | 0.4 | |
| 15 | 0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③⑤ | C. | ②④⑥ | D. | ④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M、N的简单离子半径:r(N-)>r(M2-) | |
| B. | 气态氢化物的稳定性:M>X | |
| C. | X、Y形成的化合物中只有离子键 | |
| D. | X、Y、N所形成化合物的水溶液可能显中性或碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com