
����Ŀ����������ƣ�Na2S2O35H2O��ʽ��248�����������մ��ֳ�Ϊ��������������������ҵ�����ͼ���Ҳ������ֽ��Ư��������������������ˮ���������Ҵ������ȡ�������ֽ⣬��ҵ�ϳ����������Ʒ�������Ʊ���ijʵ��ģ�ҵ���ȡ��������ƣ��䷴Ӧװ�ü������Լ���ͼ1��
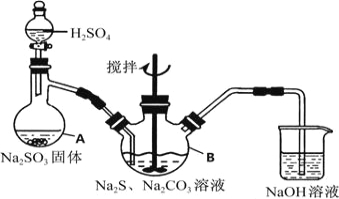
ͼ1
ʵ������������Ϊ��
�ٿ�����Һ©����ʹ�����������£��ʵ����ڷ�Һ©���ĵ��٣�ʹ��Ӧ������SO2������ȵ�ͨ��Na2S��Na2CO3�Ļ����Һ�У�ͬʱ�����綯������������ˮԡ���ȣ���
��ֱ�������Ļ��Dz�����ʧ����������Һ��PH�ӽ�7ʱ��ֹͣͨ��SO2����
�۳��ȹ��ˣ�����Һ����Ũ������ȴ����Na2S2O35H2O
���ھ����ˡ�ϴ�ӡ�����õ������Ʒ
��1��д������A������ ���������ϴ��ʱ��Ϊ�˼��ٲ������ʧ���Լ�����
��2��Ϊ�˱�֤��������ƵIJ�����ʵ���в�������ҺPH��7���������ӷ���ʽ����ԭ��
��3�����õ��IJ�Ʒ���ܺ���Na2SO4���ʣ������ʵ�����Ʒ���Ƿ����Na2SO4����֪BaS2O3������ˮ������Ҫ˵��ʵ�����������ͽ���
��4���ⶨ��Ʒ����
��ȷ��ȡ1.00g��Ʒ������������ˮ�ܽ⣬�Ե�����ָʾ����0.1000molL��1��ı���Һ�ζ�����Ӧԭ��Ϊ2S2O32��+I2=S4O32��+2I�����ζ���ʼ���յ�ĵζ���Һ��λ����ͼ�����ĵ�ı���Һ���Ϊ mL����Ʒ�Ĵ���Ϊ %
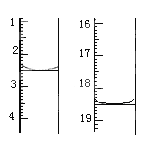
�����ζ�ʱ����֣��տ�����Һ�ֲ���ɫ��ֹͣ�ζ������ʹ��Ʒ��Na2S2O35H2O�����������IJ������________(�ƫ�ߡ���ƫ�͡����䡱)��
��5��Na2S2O3������������������Һ���ױ�Cl2����SO42�����÷�Ӧ�����ӷ���ʽΪ�� ��
���𰸡���1��������ƿ���Ҵ�����2��S2O32-+2H+=S+SO2��+H2O����3��ȡ�����ȼ������������ữ�����ˣ�ȡ����Һ������Ȼ�����Һ�������ְ�ɫ������˵���������������ʣ��������ְ�ɫ������˵��������������������4����16.00��79.36����ƫ������5��S2O32��+ 4Cl2 + 5H2O = 2SO42�� + 8Cl�� + 10H+ ��
��������
�����������1������AΪ������ƿ���������⣬���������������ˮ���������Ҵ������Ϊ�˼��ٲ������ʧ���Ҵ�����ϴ�ӣ���2��������������ᷴӦ��S2O32-+ 2H+ == S + SO2 ��+H2O����3��ȡ�����ȼ������������ữ�����ˣ�ȡ����Һ������Ȼ�����Һ�������ְ�ɫ������˵���������������ʣ��������ְ�ɫ������˵��������������������4��������ͼ2���ζ�ǰ�Ķ�����2.50mL���ζ��������18.50mL��������ĵ�����Ϊ(18.50��2.50)mL = 16.00mL���������ӷ�Ӧ����ʽ��n(Na2S2O3) = 16.00 �� 10��3 �� 0.1000 �� 2mol = 3.2 �� 10��3mol��m(Na2S2O3��5H2O) = 3.2 �� 10��3 �� 248g = 0.7936g������Ϊ0.7936/1 �� 100% = 79.36%���ھֲ���ɫ��˵������I2�������٣���Ĵ���ƫ�ͣ���5��������Ϣ����������������ת���Cl����Na2S2O3����ԭ������������SO42�������û��ϼ۵�������������ƽ�������ӷ�Ӧ����ʽΪ��S2O32��+ 4Cl2 + 5H2O == 2SO42�� + 8Cl�� + 10H+ ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У�����ȷ����
A. �ⵥ���������˷���������Ӽ�������
B. ���ʯ��ʯī������̼����̼Ԫ�ص�ͬ��������
C. Ŀǰ��ѧ�һ���ʵ�ֶ�ԭ�ӻ���ӵIJ���
D. HCl��������ˮ���ۼ����ƻ����Ӷ��γ���H+��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�������Ⱦ��������ǻ�����һ����Ҫ����������Ӧ�úʹ������Ļ��������������������Ҫ���塣
I����Ⱦ��SO2��NOx��O2Ԥ��������CaSO3����Һ���գ��ɼ���β����SO2��NOx�ĺ�����T��ʱ��O2����������SO2��NOx����Ҫ��Ӧ���Ȼ�ѧ����ʽΪ��
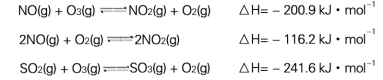
(1) T��ʱ����Ӧ3NO(g)+O3(g)![]() 3NO2��g������H= kJ��mol��1��
3NO2��g������H= kJ��mol��1��
(2) T��ʱ����0.6 mol NO��0.2 molO3������뵽2L�̶��ݻ��ĺ����ܱ������У�NO��Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ��
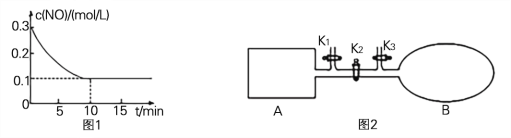
�� T��ʱ����Ӧ3NO(g) +O3 (g) ![]() 3NO2 (g)��ƽ�ⳣ��K= ��
3NO2 (g)��ƽ�ⳣ��K= ��
�� ����˵����Ӧ�ﵽƽ��״̬���� ����д��ĸ����
A��������ɫ���ٸı� B�������ƽ��Ħ���������ٸı�
C��������ܶȲ��ٸı� D����λʱ��������O3��NO2���ʵ���֮��Ϊ1��3
II��NO2�Ķ�����N2O4�ǻ���г���������������������⣺
(3) ��ͼ2��ʾ��A���ɵ��Ȳ����Ƴɵĺ����ܱ�������B��һ�ͻ�ѧ��ʴ�����ڴ��ȵ������ҡ��ر�K2������1 molNO2ͨ��K1��K3�ֱ�������A��B�У���Ӧ��ʼʱA��B�������ͬ��ΪaL�����Ե����е������������
�� ����A�е���ƽ������ʱ��ts���ﵽƽ���������ѹǿΪ��ʼѹǿ��0.8������ƽ����ѧ��Ӧ����v(NO2)= ��
�� ƽ�����A�������ٳ���0.5 mol N2O4�������µ���ƽ���ƽ��������NO2��������������������������С�������������� ��
�� ����ƽ���K2�����µ�����ƽ�⣬B���ҵ����Ϊ0.8aL�����ڴ�K2֮ǰ������B�����Ϊ L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����aLAl2(SO4)3��(NH4)2SO4�Ļ����Һ�ֳ����ȷݣ�����һ������bmolBaCl2��ǡ��ʹ��Һ�е�SO42-������ȫ��������һ����������ǿ����ȿɵõ�c molNH3���壬��ԭ��Һ�е�Al3+������Ũ��(mol/L)Ϊ�� ��
A��![]() B��
B��![]() C��
C��![]() D��
D��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ����Ľṹ��ʽΪ![]() ��
��
��1�����й���ˮ�����������ȷ����_______________��
A��![]() ��
��![]() ��Ϊͬϵ��
��Ϊͬϵ��
B��ˮ�������������ԭ��һ������ͬһƽ����
C��ˮ����ȿ��Կ����Ƿ������ʣ�Ҳ���Կ���������������
��2����ˮ������___________________��Һ���ã���������![]() ����д����
����д����![]() ת��Ϊ
ת��Ϊ![]() �Ļ�ѧ����ʽ_______________��
�Ļ�ѧ����ʽ_______________��
��������������֪ij��������Է�������Ϊ124��������KMnO4��Һ�������õ����ֲ��a��CH3COOH�� b��![]()
��3��b������Ϊ________________��
��4�������ķ���ʽΪ________________��д���������ܵĽṹ��ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в��������ӷ�Ӧ����
A. ������������ȼ�� B. ���������������Һ��Ӧ
C. ��������ͭ��Һ��Ӧ D. ����ʯ��ϡ���ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����ǵ��������������أ������������������ǣ� ��
A. ����������ӵ�ʳ���еĵ���أ�KIO3��
B. ���м�����±����Ҫ�ɷ�ΪMgCl2����������
C. �����պ�����ζ�ķ���������֯��ʹ�ë֯��
D. ����ˮ�м��������������ɳ�ȥ���е�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�����ڱ��ж����ڵ�һ���֣���֪A��C����Ԫ�صĺ˵����֮�͵���B�ĺ˵����������������ȷ���ǣ�������
A | C | |
B |
A.BΪ�ڶ����ڵ�Ԫ��
B.CΪ��������Ԫ��
C.A��ԭ������Ϊ6
D.C�Ƿǽ�������ǿ��Ԫ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com