
| A. | N2O5 | B. | NO | C. | NO2 | D. | N2O3 |
分析 设氮气和水的物质的量分别为5mol、6mol,根据H原子守恒计算氨气物质的量,再根据N原子守恒、O原子守恒计算氧化物中N、O原子物质的量,进而确定氧化物化学式.
解答 解:设氮气和水的物质的量分别为5mol、6mol,根据H原子守恒,可知氨气物质的量为$\frac{6mol×2}{3}$=4mol,
根据N原子守恒,可知氧化物中N原子物质的量为5mol×2-4mol=6mol,
根据O原子守恒,可知氧化物中O原子物质的量为6mol,
故氧化物中N、O原子数目之比为6mol:6mol=1:1,
故该氧化物化学式为NO,
故选B.
点评 本题考查反应方程式有关计算,难度不大,关键是对质量守恒定律的理解.


科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Fe3+、OH-、Cl- | B. | Mg2+、Na+、Cl-、SO42- | ||
| C. | NH4+、Ba2+、NO3-、OH- | D. | H+、K+、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯分子里所有的原子在同一平面上 | |
| B. | 乙烯的结构简式为CH2CH2,电子式为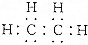 | |
| C. | 乙烯分子中碳氢键之间的夹角约为120° | |
| D. | 乙烯分子中既含有极性键又含有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
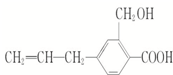 某有机物的结构简式为如右图所示,其可能具有的性质是( )
某有机物的结构简式为如右图所示,其可能具有的性质是( ) | A. | 全部 | B. | 仅能发生①②③④ | C. | 除⑤外都能 | D. | 除④⑤外都能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ•mol-1,则H2O(g)?H2O(l) 的△H=40.69 kJ•mol-1 | |||||||||||
| B. | 已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)•c(CO32-)=6.82×10-6 | |||||||||||
| C. | 已知:
| |||||||||||
| D. | 已知CaCO3 (s)?CaO(s)+CO2(g)△H>0,则低温有利于该反应的自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 molAl3+含有的核外电子数为3NA | |
| B. | 将58.5g NaCl溶于1.00 L水中,所得NaCL溶液的浓度为1.00mol•L-1 | |
| C. | 1 molCl2与足量的铁反应,转移的电子为数3Na | |
| D. | 常温下,10LpH=1的硫酸溶液中含有的H+离子数为NA. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:a>b>c>d | B. | 离子的还原性:Y2->Z- | ||
| C. | 氢化物的稳定性H2Y>HZ | D. | 原子半径X<W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com