
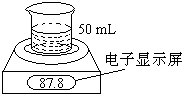
 ijѧ���õ�����ƽ�ͱ�Ҫ�Ļ�ѧʵ�������ⶨ�����Ͻ��и���ֺ�������ʵ��װ����ͼ��ʾ��ʵ��ʱ��ȡһ�������Ͻ𣬽����г�����ȫ�����뵽ʢ��50mL 5.0mol?L-1 NaOH��Һ���ձ��У��Իش��������⣺
ijѧ���õ�����ƽ�ͱ�Ҫ�Ļ�ѧʵ�������ⶨ�����Ͻ��и���ֺ�������ʵ��װ����ͼ��ʾ��ʵ��ʱ��ȡһ�������Ͻ𣬽����г�����ȫ�����뵽ʢ��50mL 5.0mol?L-1 NaOH��Һ���ձ��У��Իش��������⣺| ʵ��������� | ʱ��/min | ������ƽ�Ķ���/g |
| �ձ�+NaOH��Һ | 80.0 | |
| �ձ�+��Һ+��Ʒ | 0 | 87.8 |
| 1 | 87.5 | |
| 2 | 87.3 | |
| 3 | 87.2 | |
| 4 | 87.2 |
| 7.8g-5.4g |
| 7.8g |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��18gD2O�к������ӵ���ĿΪNA |
| B����״���£�11.2L�������ϩ�Ļ����������ԭ�ӵ���ĿΪ2NA |
| C��1L0.1mol?L-1CH3COOH��Һ�к��з��ӵ���ĿС��0.1NA |
| D��1L0.5 mol?L-1Na2CO3��Һ�к���CO32-����ĿΪ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��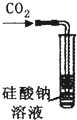 ��װ�ã�������֤��̼�ķǽ����Աȹ�ǿ |
B��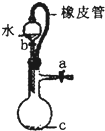 ��װ�ã���Ƥ�ܵ�������ƽ��ѹǿ��ʹˮ˳������ |
C��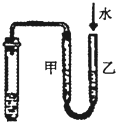 ��װ�ã���ͼʾ�ķ����ܼ���װ�õ������� |
D�� ��װ�ã����ռ�������̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
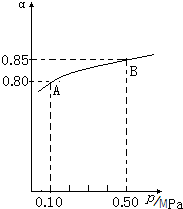 SO2��NOx�ڻ�ѧ��ҵ������Ҫ��;��Ҳ�Ǵ�����Ⱦ����Ҫ��Դ�����������ò��أ�Ԥ�������������ǵ�ǰ��ҵ�Ϻͻ������������о�����Ҫ����֮һ��
SO2��NOx�ڻ�ѧ��ҵ������Ҫ��;��Ҳ�Ǵ�����Ⱦ����Ҫ��Դ�����������ò��أ�Ԥ�������������ǵ�ǰ��ҵ�Ϻͻ������������о�����Ҫ����֮һ��| ���� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ�����У�������ѹǿ�����SiCl4��ת���� |
| B������Ӧ��ʼʱSiCl4Ϊ1 mol�����ƽ��ʱ����������ΪQ kJ |
| C������λʱ��������x molHCl��ͬʱ������x molH2����Ӧ�ﵽƽ��״̬ |
| D��ʹ�ù�����H2�������¶ȶ��������SiCl4��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����Ϸ�Ӧ | B���ֽⷴӦ |
| C���û���Ӧ | D�����ֽⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� �� | X | Y | Z | Q |
| ��Ӧǰ����/g | 2 | 2 | 84 | 5 |
| ��Ӧ������/g | ���� | 24 | 0 | 14 |
| A�����Ϸ�Ӧ | B���û���Ӧ |
| C���ֽⷴӦ | D�����ֽⷴӦ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com