
| A. | 步骤②发生的主要反应为:2Fe2++H2O2+2H+=2Fe3++2H2O | |
| B. | 步骤②可用氯水、硝酸等强氧化剂代替H2O2 | |
| C. | 步骤③用 CuCO3代替CuO也可调节溶液的pH | |
| D. | 步骤⑤的操作为:向漏斗中加人少量冷的蒸馏水至浸没晶体,待水自然流下,重复操作 2~3次 |
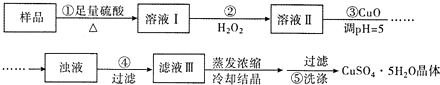
分析 由实验流程可知,样品与足量硫酸反应,生成硫酸铜和硫酸亚铁,加入过氧化氢,发生氧化还原反应生成硫酸铁,然后加入CuO调节溶液的pH,使Fe3+水解而生成Fe(OH)3沉淀,得到硫酸铜溶液,经蒸发浓缩、冷却结晶得到硫酸铜晶体,以此来解答.
解答 解:由实验流程可知,样品与足量硫酸反应,生成硫酸铜和硫酸亚铁,加入过氧化氢,发生氧化还原反应生成硫酸铁,然后加入CuO调节溶液的pH,使Fe3+水解而生成Fe(OH)3沉淀,得到硫酸铜溶液,经蒸发浓缩、冷却结晶得到硫酸铜晶体,
A.步骤②为亚铁离子与过氧化氢的氧化还原反应,离子反应为2Fe2++H2O2+2H+=2Fe3++2H2O,故A正确;
B.步骤②可用氯水、硝酸等强氧化剂代替H2O2,引入杂质氯离子、硝酸根离子等,难以除去,故B错误;
C.CuCO3和CuO都与溶液中H+反应,起到调节溶液pH的作用,并不引入新的杂质,故C正确;
D.步骤⑤为洗涤固体,固体具有吸附性,过滤时表面有可溶性物质,则操作为向滤出晶体的漏斗中加少量水浸没晶体,自然流下,重复2-3次,可洗涤晶体,故D正确;
故选B.
点评 本题考查硫酸铜的制备实验,为高频考点,把握制备流程中的反应、混合物分离提纯方法等为解答的关键,侧重分析与实验能力的考查,题目难度中等,注意氧化还原反应及盐类水解等原理的应用和分析.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 在相同的条件下,2mol氢气与1 mol氧气的总能量小于2mol 水蒸气的总能量 | |
| B. | H2(g)+$\frac{1}{2}$ O2(g)→H2O(1)+Q1;Q1>241.8kJ | |
| C. | 氢气燃烧是放热反应,所以氢气和氧气反应不需要其他外界条件即可发生 | |
| D. | 任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学习小组探究NaHCO3、Na2HCO3和盐酸(盐酸浓度均为1mol.L-1)反应过程中的热效应,实验测得如下数据:
某学习小组探究NaHCO3、Na2HCO3和盐酸(盐酸浓度均为1mol.L-1)反应过程中的热效应,实验测得如下数据:| 序号 | 35mL试剂 | 固体 | 混合温度前/℃ | 混合温度后/℃ |
| ① | 水 | 2.5gNaHCO3 | 20.0 | 18.5 |
| ② | 水 | 3.2gNa2CO3 | 20.0 | 24.3 |
| ③ | 盐酸 | 2.5gNaHCO3 | 20.0 | 16.2 |
| ④ | 盐酸 | 3.2gNa2CO3 | 20.0 | 25.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
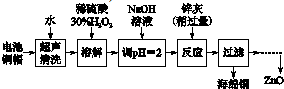
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com