
| A. | 在同温同压时,相同体积的任何气体单质所含的原子数目相同 | |
| B. | 2 g氢气所含原子数目为NA | |
| C. | 在常温常压下,11.2 L氮气所含的原子数目为NA | |
| D. | 17 g氨气所含原子数目为4 NA |
分析 A、气体单质分为单原子分子、双原子分子和多原子分子;
B、氢气由氢原子构成;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、求出氨气的物质的量,然后根据氨气中含4个原子来分析.
解答 解:A、气体单质分为单原子分子、双原子分子和多原子分子,故同温同压下,相同体积的任何气体单质的物质的量相同,但含有的原子个数不一定相同,故A错误;
B、氢气由氢原子构成,故2g氢气中含有的氢原子的物质的量为2mol,个数为2NA个,故B错误;
C、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氮气的物质的量小于0.5mol,则含有的氮原子小于NA个,故C错误;
D、17g氨气的物质的量为1mol,而氨气中含4个原子,故1mol氨气中含4NA个原子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ②⑧ | B. | ①⑥ | C. | ②④ | D. | ③⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3+CaCl2═CaCO3↓+2NaCl | B. | Fe+CuSO4═Cu+FeSO4 | ||
| C. | CaO+H2O═Ca(OH)2 | D. | NaOH+HCl═NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 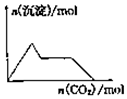 向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量 | |
| B. | 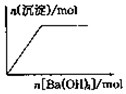 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 | |
| C. | 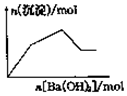 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量 | |
| D. | 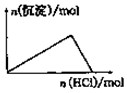 向NaAlO2溶液中逐滴加入盐酸至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
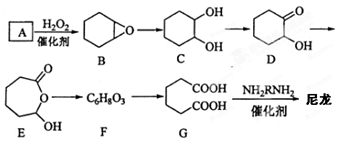
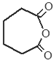 .
. .
.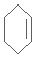 $\stackrel{Br_{2}/CCl_{4}}{→}$
$\stackrel{Br_{2}/CCl_{4}}{→}$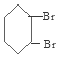 $→_{△}^{NaOH/C_{2}H_{5}OH}$
$→_{△}^{NaOH/C_{2}H_{5}OH}$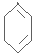 .
.查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
相同体积、相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )
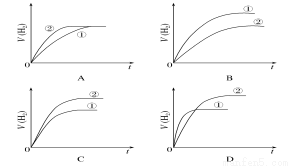
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
从植物花汁中提取的一种有机HIn,可做酸碱指示剂,在水溶液中存在电离平衡:HIn(红色)  H++In-(黄色),对上述平衡解释不正确的是
H++In-(黄色),对上述平衡解释不正确的是
A.升高温度平衡向正方向移动
B.加入盐酸后平衡向逆方向移动,溶液显红色
C.加入NaOH溶液后平衡向正方向移动,溶液显黄色
D.加入NaHSO4溶液后平衡向正方向移动,溶液显黄色
查看答案和解析>>
科目:高中化学 来源:2017届安徽省黄山市高三上月考二化学卷(解析版) 题型:选择题
某同学组装了如图所示的电化学装置,其中电极I为Al,其它均为Cu,下列说法正确的是( )
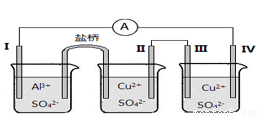
A.装Al2(SO4)3 溶液的烧杯是原电池,其余两个为电解(电镀)池
B.盐桥中电子从右侧流向左侧
C.电极II逐渐溶解
D.电极IV的电极反应:Cu2+ + 2e- = Cu
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com