
【题目】2017年5月5日,中国首架按照国际标准研制,拥有自主知识产权的大型客机C-919在上海浦东机场首飞,科学家在实验室研究利用催化技术将飞机尾气中的NO和CO转变成CO2和N2,其反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
(1)上述反应的熵变ΔS_________(填“>”“<”或“=”,下同)0,该反应能够自发进行,则反应的ΔH_______0。
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是____________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(3)若将1 molNO和2 mol CO通入2 L的恒容密闭容器中,在一定条件下发生上述反应,反应中生成的N2的物质的量浓度随时间的变化情况如图1所示。则NO从反应开始到平衡时的平均反应速率v(NO)=_________,4 min末CO的浓度为_________________。
(4)已知上述反应中NO的平衡转化率与压强、温度的关系如图2所示。工业上催化装置比较适合的温度和压强是____________________。

(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
实验编号 | T(K) | NO的初始浓度 (mol·L-1) | CO的初始浓度 (mol·L-1) | 催化剂的比表面积 (m2·g-1) |
I | 400 | 1.20×10-3 | 3.80×10-3 | 75 |
Ⅱ | 400 | 1.20×10-3 | 3.80×10-3 | 100 |
Ⅲ | 450 | 1.20×10-3 | 3.80×10-3 | 100 |
请在图3中分别画出上表中实验Ⅱ、Ⅲ条件下混合气体中NO的浓度随时间变化的曲线,并标明各条曲线的实验编号__________。

【答案】 < < CD 0.05 molL-1·min-1 0.8 molL-1 400 K,1 MPa 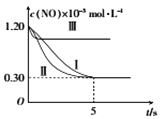
【解析】(1)正反应体积减小,则上述反应的熵变ΔS<0;该反应能够自发进行,根据△G=△H-T△S<0可以自发进行可知反应的ΔH<0。(2)A.选用更有效的催化剂不能改变平衡状态,转化率不变,A错误;B.正反应放热,升高反应体系的温度平衡向逆反应方向进行,转化率降低;C. 正反应放热,降低反应体系的温度,平衡向正反应方向进行,转化率升高,C正确;D.缩小容器的体积增大压强,平衡向正反应方向进行,转化率升高,D正确,答案选CD;(3)根据图像可知平衡时生成氮气是0.1mol/L,根据方程式可知消耗NO是0.2mol/L,则NO从反应开始到平衡时的平均反应速率v(NO)=0.2mol/L÷4min=0.05 molL-1·min-1;消耗CO是0.2mol/L,则4 min末CO的浓度为1mol/L-0.2mol/L=0.8mol/L。(4)根据图像可知常压下转化率已经很高,相同压强下400K时的转化率高于500K时的转化率,因此工业上催化装置比较适合的温度和压强是400 K,1 MPa。(5)催化剂改变反应速率,不能改变平衡状态,又因为在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率,且正反应放热,升高温度平衡向逆反应方向进行,所以图像为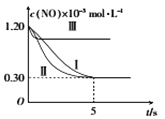 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】共价键、离子键、分子间作用力都是粒子间的作用力,含有以上两种作用力的晶体是( )
A. SiO2 B. CCl4 C. NaCl D. 金刚石
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如下图所示.则下列离子组在对应的溶液中,一定能大量共存的是
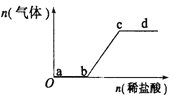
A. a点对应的溶液中:Na+、OH-、SO42-、NO3-
B. b 点对应的溶液中:Al3+、Fe3+、MnO4-、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D. d 点对应的溶液中:F-、NO3-、Fe3+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D,4种元素,已知A﹣核外有18个电子;B原子最外层电子数比D原子核外电子数多2个,B原子比D原子多2个电子层;D+核外没有电子,C元素原子核外电子数比B元素原子核外电子数多5个.
(1)写出四种元素的名称:
A、B、C、D
(2)画出C和D原子的结构示意图 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 石油裂化的目的是为了得到气态短链烃
B. 苯与溴的四氯化碳溶液充分混合仅发生萃取
C. 相同温度下,酯在酸性环境下的水解程度小于碱性环境
D. 煤的干馏是指煤在空气中加强热发生复杂的物理、化学变化的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确且能合理解释亊实的是
A. SO2随雨水降落.形成酸雨:SO2+ H2O = 2H+ + SO32-
B. 向Mg(HCO3)2溶液中加人过量NaOH溶液,产生白色沉淀:Mg2+ +2HCO3- +2OH -= MgCO3↓+2H2O
C. 向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置—段时间后,溶液变蓝: 4H++4I-+O2=2I2+2H2O
D. Cl2通入FeCl2 溶液中生成 FeCl3:Fe2++Cl2=2Cl-+Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组为探究ClO﹣、I2、SO42﹣在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下:
实验①:在淀粉KI溶液中加入少量NaClO溶液,并加入少量的稀H2SO4 , 溶液立即变蓝;
实验②:向实验①的溶液中加入4L 0.5mol/L的Na2SO3溶液,发生反应如下
SO32﹣+I2+H2O→SO42﹣+I﹣+H+(未配平),恰好完全反应.
(1)以上实验说明,在酸性条件下ClO﹣、I2、SO42﹣的氧化性由弱到强的顺序是
(2)实验②中化学反应转移电子的物质的量是 .
(3)写出实验①中发生反应的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com