
| A. | 热的纯碱溶液去油污 | B. | 浓硫化钠溶液有臭味 | ||
| C. | 加热氯化铁溶液颜色变深 | D. | 过氧化钠粉末变白 |
分析 纯碱、硫化钠为强碱弱酸盐,氯化铁为强酸弱碱盐,对应的水溶液都能水解,过氧化钠粉与空气中水、二氧化碳发生反应,与盐类水解无关,据此进行解答.
解答 解:A.碳酸钠中弱离子碳酸根的水解导致溶液显碱性,碱性溶液能去除油污,与盐类水解有关,故A错误;
B.硫化钠中的硫离子水解会获得具有臭鸡蛋气味的硫化氢,与盐类水解有关,故B错误;
C.三价铁水解受温度的影响,温度越高水解程度越大,生成的氢氧化铁越多,颜色变深,与盐类水解有关,故C错误;
D.过氧化钠为淡黄色,过氧化钠与空气中水、二氧化碳反应后变为白色,发生了化学反应,该变化与盐的水解无关,故D正确;
故选D.
点评 本题考查了盐的水解原理及其应用,题目难度不大,明确盐的水解原理及其影响为解答关键,注意过氧化钠的化学性质,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:解答题
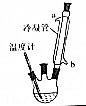 肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下:
肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下: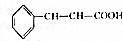 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$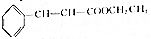 +H2O
+H2O | 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 乙醇 | 46 | 0.789 | 78.3 | 与水互溶 |
| 肉桂酸 | 148 | 1.245 | 300 | 微溶于水 |
| 肉桂酸乙酯 | 176 | 1.049 | 270 | 不溶于水 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐水蒸发结晶,蒸发皿中出现大量晶体时停止加热,利用余热使溶液蒸干 | |
| B. | 金属钠着火,立即用沙土扑灭 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 实验室制取蒸馏水的装置中,冷水从冷凝管的上口进,下口出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
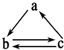 下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )| 物质 选项 | a | b | c |
| A | SiO2 | Na2SiO3 | H2SiO3 |
| B | C | CO | CO2 |
| C | Fe | FeCl2 | FeCl3 |
| D | CuO | Cu(OH)2 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  根据图可判断可逆反应A2(g)+3B2(g)═2AB3(g)的△H>0 | |
| B. | 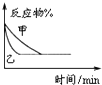 表示压强对可逆反应2A(g)+2B(g)═3C(g)+D(s)的影响,乙的压强大 | |
| C. | 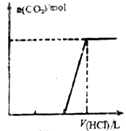 表示在含等物质的量NaOH、Na2CO3的混合溶液中逐滴加入0.1mol/L盐酸至过量时,产生气体的物质的量与消耗盐酸的体积关系 | |
| D. | 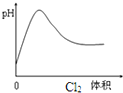 表示Cl2通入H2S溶液中pH变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径由大到小:Z2->X+>Y3+>W2- | |
| B. | 气态氢化物的稳定性:H2W强于H2Z | |
| C. | 工业上常采用电解法冶炼Y 单质 | |
| D. | W、X 形成的化合物中阴、阳离子个数比一定是1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | Na2B2O7 | CaF2 | H3BO3 | NH3 |
| A | 原子晶体 | 金属晶体 | 原子晶体 | 分子晶体 |
| B | 离子晶体 | 分子晶体 | 离子晶体 | 分子晶体 |
| C | 离子晶体 | 离子晶体 | 分子晶体 | 分子晶体 |
| D | 分子晶体 | 离子晶体 | 分子晶体 | 离子晶体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池的正极反应式为H2+2OH--2e-═2H2O | |
| B. | 用铂电极电解硫酸铜溶液的阳极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 表示醋酸与NaOH的稀溶液反应的中和热的化学方程式为H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ.mol-1 | |
| D. | NaHSO3溶于水时水解的离子方程式为HSO3-+H2O?SO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b>c | B. | c>a>b | C. | b>a>c | D. | a>c>b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com