
| A、13C与14C |
| B、CH3CH2OH与CH3COOH |
| C、甲烷与丙烷 |
| D、CH3CH2CH2CH3与 CH3CHCH3CH3 |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
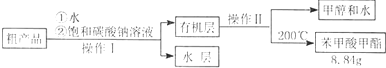
查看答案和解析>>
科目:高中化学 来源: 题型:
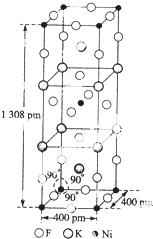 尿素(H2NCONH2 )可用于制有机铁肥.主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]
尿素(H2NCONH2 )可用于制有机铁肥.主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]查看答案和解析>>
科目:高中化学 来源: 题型:
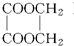 以乙醇为原料,用下述6种类型的反应:来合成乙二酸乙二酯(如图)的正确顺序是( )
以乙醇为原料,用下述6种类型的反应:来合成乙二酸乙二酯(如图)的正确顺序是( )| A、①⑤②③④ |
| B、①②③④⑤ |
| C、②③⑤①④ |
| D、②③⑤①⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
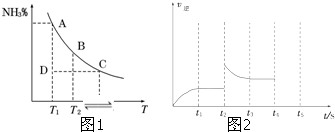
| c(X)?c2(Y) |
| c2(Z)?c2(W) |
| A、该反应可表示为X(g)+2Y(g)?2Z(g)+2W(g) |
| B、减小X浓度,该反应速率一定减小,平衡向逆反应方向移动 |
| C、增大反应容器的压强,平衡常数K减小 |
| D、升高温度,W(g)体积分数增加,则正反应是放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com