
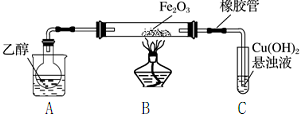
分析 (1)装置中BC之间无防倒吸的装置,需要增加防倒吸装置,可以在导气管末端连接一个干燥管,细管短插入氢氧化铜悬浊液;
(2)水浴加热或对烧杯进行加热可以快速得到乙醇气体;
(3)④依据铁离子的实验检验方法分析,铁离子加入硫氰酸钾溶液会变红色;利用亚铁离子具有还原性可以被高锰酸钾溶液氧化检验;乙醇和氧化铁反应过程中可能会生成铁或四氧化三铁,能被磁铁吸引;
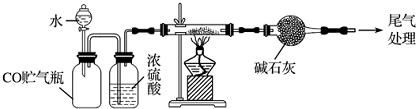
(4)先组装装置,检验装置气密性,加入试剂,加入水把一氧化碳赶入后续装置,点燃酒精灯加热玻璃管,反应结束后停止加热,关闭分液漏斗活塞;
玻璃管称量剩余固体,依据质量变化计算铁元素和氧元素物质的量之比;碱石灰增重n g为生成二氧化碳的质量,CO转化为CO2获得的氧原子为氧化物中O原子,再计算Fe原子物质的量,进而取得x、y关系.
解答 解:(1)装置中BC之间无防倒吸的装置,需要增加防倒吸装置,在导气管末端连接一个干燥管,将干燥管的管口插入液面下少许或将导气管管口移出溶液至液面上方,接近液面的地方等,
故答案为:在导气管末端连接一个干燥管,将干燥管的管口插入液面下少许或将导气管管口移出溶液至液面上方,接近液面的地方等;
(2)为快速得到乙醇气体,可采取的方法是:水浴加热或对烧杯进行加热,
故答案为:水浴加热或对烧杯进行加热;
(3)④依据铁离子的实验检验方法分析,铁离子加入硫氰酸钾溶液会变红色,取少量溶液加入KSCN溶液,变红色,则有Fe3+;向另一份溶液中加入酸化的高锰酸钾溶液,紫红色变浅或褪去证明含有亚铁离子;氧化铁做催化剂参与反应过程,乙醇和氧化铁反应过程中可能会生成铁或四氧化三铁,能被磁铁吸引,M中一定有+3价铁,0价和+2价铁至少有一种,选c,
故答案为:取少量溶液加入KSCN溶液,变红色,则有Fe3+;向另一份溶液中加入酸化的高锰酸钾溶液,紫红色变浅或褪去证明含有亚铁离子;c;
(4)先组装装置,检验装置气密性,加入试剂,加入水把一氧化碳赶入后续装置,点燃酒精灯加热玻璃管,反应结束后停止加热,关闭分液漏斗活塞,玻璃管称量剩余固体,依据质量变化计算铁元素和氧元素物质的量之比,正确的操作顺序是:①⑤③④②⑥⑦⑧,选b,
碱石灰增重n g为生成二氧化碳的质量,CO转化为CO2获得的氧原子为氧化物中O原子,则氧化物中O原子物质的量为$\frac{ng}{44g/mol}$=$\frac{n}{44}$molmol,Fe原子物质的量为$\frac{mg-\frac{b}{44}mol×16g/mol}{56g/mol}$,则x:y=$\frac{mg-\frac{b}{44}mol×16g/mol}{56g/mol}$:$\frac{n}{44}$mol=$\frac{11m-4n}{14n}$,
故答案为:b;$\frac{11m-4n}{14n}$.
点评 本题考查了物质性质的实验探究和物质组成的分析判断,实验操作步骤的设计和完善,实验过程中的反应实质分析判断,现象的理解和应用是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 3.2gO2、O3组成的混合物中含有的质子数为1.6NA | |
| B. | 当反应6HCl+KClO3═Cl2↑+KC1+3H2O有71gC l2生成时,转移电子数目为2NA | |
| C. | 1molC2H4分子中含共用电子对的数自为5NA | |
| D. | 0.1mol乙醇与足量乙酸充分反应后,生成的水分子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
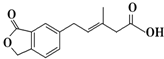
| A. | M可以发生加成、加聚、水解、酯化等反应 | |
| B. | 1mol M最多可以与3mol NaOH反应 | |
| C. | M苯环上的一氯取代物有三种不同结构 | |
| D. | 1mol M最多可以与5mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 拉瓦锡研究了空气的成分,让大家认识了氧气 | |
| B. | 图为雾霾的主要成分示意图,汽车尾气的大量排放是造成雾霾天气的人为因素之一 | |
| C. | “滴水石穿、绳锯木断、落汤螃蟹着红袍”均不包含化学变化 | |
| D. | “看似风平浪静,实则暗流涌动”形象地描述了溶解平衡的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol羟基与17 g NH3所含电子数都为NA | |
| B. | 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32 g | |
| C. | 常温常压下,28 g C2H4、C3H6的混合气体中含有碳原子的数目为2NA | |
| D. | 适量铜粉溶解于1 L 0.5 mol•L-1稀硝酸中,当生成2.24 L NO时,溶液中氮原子数为0.4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

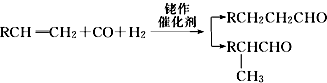
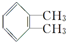 ,名称为邻二甲苯.
,名称为邻二甲苯.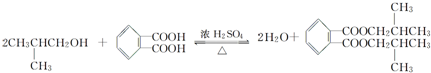 .
.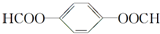 ; 1molX与NaOH溶液共热反应,最多消耗4molNaOH.
; 1molX与NaOH溶液共热反应,最多消耗4molNaOH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| B. | 分子组成相差一个或几个CH2原子团的化合物必定互为同系物 | |
| C. | 同系物的分子量数值一定相差14的整数倍 | |
| D. | 同系物的化学性质相似,物理性质随碳原子数的递增呈现规律性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z的气态氢化物稳定性强于其它的非金属气态氢化物 | |
| B. | 原子半径:Z>Y>X | |
| C. | CaY2与水发生氧化还原反应时,CaY2只作氧化剂 | |
| D. | CaX2、CaY2和CaZ23种化合物中,阳离子与阴离子个数比均为1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com