
【题目】为了将混有K2SO4、MgSO4、CaCl2的KCl固体提纯,并制得纯净的KCl晶体,某同学设计如下实验方案,请回答下列问题:

(1)操作⑤⑥的名称依次为___、___。
(2)操作②、③加入溶液后,发生反应的离子方程式分别为___、___。
(3)该同学设计的实验方案___(填“严密”或“不严密”),理由是___,该步骤所加试剂应该是___。
【答案】过滤 蒸发结晶 Ba2++SO42-=BaSO4↓ Mg2++2OH-=Mg(OH)2↓ 不严密 加入硝酸会引入杂质NO3- 盐酸
【解析】
由实验流程可知,除去SO42-、Ca2+、Mg2+离子使它们分别形成BaSO4、CaCO3、Mg(OH)2沉淀,需要加入稍过量的BaCl2、K2CO3、KOH溶液,过量的Ba2+可用K2CO3溶液除去,因此实验时必须先加入Ba(NO3)2溶液,后加入K2CO3溶液,则试剂顺序为BaCl2、KOH、K2CO3或KOH、BaCl2、K2CO3或BaCl2、K2CO3、KOH,本题采用的试剂顺序为BaCl2、KOH、K2CO3,操作①为溶解,⑤为过滤,应加稀盐酸调节溶液的pH,否则会引入杂质,⑥为蒸发结晶得到KCl。
(1)分析可知,操作⑤⑥的名称依次为过滤、蒸发;
(2)操作②、③加入的试剂为BaCl2、KOH,涉及反应的离子方程式为Ba2++SO42-=BaSO4↓、Mg2++2OH-=Mg(OH)2↓;
(3)由分析,不能利用硝酸调节pH,应加盐酸调节pH,除去过量的KOH、K2CO3。故答案为:不严密,加入硝酸会引入杂质NO3-,盐酸。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.常温常压下,11.2L氧气所含的原子数为NA
B.1.8gNH4+离子中含有的电子数为NA
C.常温常压下,48gO3含有的氧原子数为NA
D.5.6g金属铁与足量氯气充分反应时失去的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体的组成可表示为H2C2O4·xH2O,为了测定x值,进行下述实验:
①称取n g草酸晶体配成100.00 mL水溶液;
②取25.00 mL所配制的草酸溶液置于锥形瓶中,加稀硫酸,用浓度为a mol·L-1的KMnO4溶液滴定,试回答下列问题:
(1)写出滴定实验中所发生反应的化学方程式:_______________
(2)实验中KMnO4溶液应装在____式滴定管中,滴定终点的判断依据是________________
(3)滴定过程中用去V mL a mol·L-1的KMnO4溶液,则所配制的草酸的物质的量浓度为_______mol·L-1
(4)若滴定终点读数时目光俯视,则计算出的x值可能___________(填偏大、偏小、无影响)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用HCl气体或NaOH固体调节0.01mol·L-1二元酸(以H2A表示)溶液的pH(忽略溶液体积的变化),溶液中H2A、HA-、A2-、H+、OH-浓度的对数值(lgc)变化如下图所示:
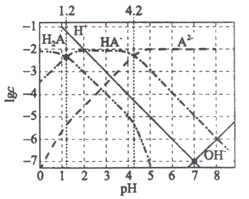
下列说法错误的是
A. 25℃时,H2A的Ka1数量级为10-2
B. pH=1.2时,调节溶液pH用的是HCl气体
C. pH=7时,溶液中:c(Na+)=c(HA-)+c(A2-)
D. pH=8时,溶液中:c(A2-)>c(HA-)>c(H2A)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根皮素R( )可应用于面膜、护肤膏霜和精华素中。其中一种合成R的路线如下:
)可应用于面膜、护肤膏霜和精华素中。其中一种合成R的路线如下:

已知
①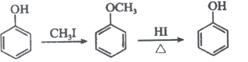
②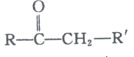 +R’’CHO
+R’’CHO +H2O
+H2O
(1)A的化学名称是___________,B→C的反应类型是___________。
(2)D的结构简式是___________,其核磁共振氢谱共有___________组峰。
(3)E→F的化学方程式为___________,G的官能团的名称是___________。
(4)G→H的化学方程式为______________________。
(5)M是F的同分异构体,同时符合下列条件的M的结构有___________种(不考虑立体异构)
①1能与FeCl3溶液发生显色反应 ②能发生银镜反应
(6)设计以丙烯和1,3-丙二醛为起始原料制备![]() 的合成路线___________(无机试剂任选)。
的合成路线___________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程不能用勒夏特列原理解释的是:
A. 热的纯碱溶液洗涤油渍效果较好 B. 将AlCl3溶液蒸干、灼烧,得到Al2O3固体
C. 实验室配制FeCl3溶液时滴入盐酸 D. 制硫酸工业中,采用500℃左右氧化SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)耐高温、硬度大,可用石英与焦炭在1400~1450℃的氮气中合成:3SiO2(s)+6C(s)+2N2(g)=Si3N4(s)+6CO(g)-Q(Q>0),在一定条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列问题:
(1)上述反应所涉及的属于第三周期的元素,其原子的最外层电子轨道表示式为______。其中一种元素的原子核外s电子数与p电子数相等,其原子的核外电子能量不同的有_____种。
(2)上述反应混合物中的极性分子是______,写出非极性分子的电子式________。分析用氮化硅制造轴承和发动机中耐热部件的原因是___________。
(3)该反应的平衡常数表达式为__________。可以提高二氧化硅转化率的措施是________(任写一条),该措施对平衡常数的影响为__________(填“增大”、“减小”或“保持不变”)。
(4)测得平衡时固体质量减少了5.6g,则用氮气表示的平均反应速率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业盐中含有NaNO2,外观和食盐相似,有咸味,人若误食会引起中毒,致死量为0.3~0.5 g。已知NaNO2能发生如下反应(离子方程式已配平):2![]() +xI-+yH+===2NO↑+I2+zH2O,请回答下列问题:
+xI-+yH+===2NO↑+I2+zH2O,请回答下列问题:
(1)上述反应中,x的数值是____,根据是____________;y的数值是_____,根据是____
(2)根据上述反应,可用化学试纸及生活中常见物质进行实验来鉴别工业盐和食盐,现有淀粉碘化钾试纸,则还需选用的生活中常见物质的名称为____________。
(3)某工厂废弃液中含有2%~5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是___(填字母)。
a.NaCl b.H2O2 c.NH4Cl d.浓硫酸
所发生反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)梯恩梯(TNT)结构简式为____________________________。
(2)![]() 中含有的官能团的名称为_______________。
中含有的官能团的名称为_______________。
(3)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式________________________。
(4)某炔烃和氢气充分加成生成2,2,5-三甲基己烷,该炔烃的结构简式是________,名称是____________。
(5)分子式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为__________________
(6)分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为_______________。
(7)键线式![]() 表示的分子式为____________,名称是______________________。
表示的分子式为____________,名称是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com