
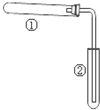
 如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )| ①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
| A、A | B、B | C、C | D、D |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、K+、Al3+、Cl-、CO32- |
| B、H+、Na+、Br-、SiO32- |
| C、Na+、Fe2+、SO42-、NO3- |
| D、K+、NH4+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 蛇纹石可用于生产氢氧化镁,简要工艺流程如下:
蛇纹石可用于生产氢氧化镁,简要工艺流程如下:| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放电时,电子从正极流向电源的负极 | |||
| B、放电时,Li+向负极移动 | |||
C、该电池的总反应为LiNiO2+6C
| |||
| D、充电时,阳极发生的电极反应为Li1-xNiO2+xLi++x e-═LiNiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
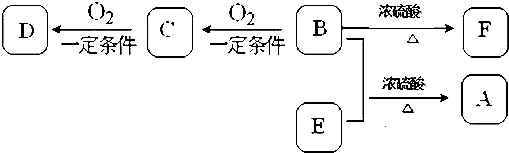
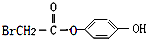 ,写出X与NaOH溶液共热的化学方程式
,写出X与NaOH溶液共热的化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
| Fe+HCl |
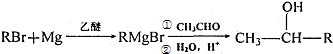
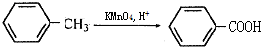
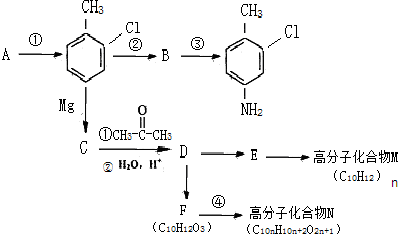
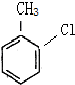 这一途径外,另一途径生成的中间产物的结构简式为
这一途径外,另一途径生成的中间产物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| n(SO32-):n(HSO3-) | 91:9 | 1:l | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
| 催化剂 |
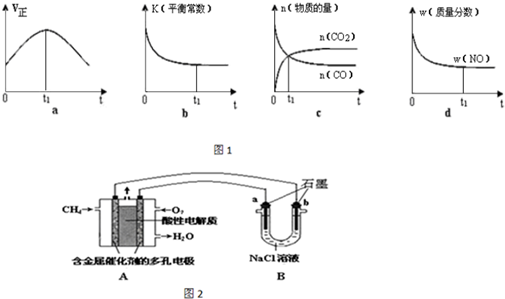
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非电解质:C6H12O6、Cl2、C2H5OH |
| B、酸性氧化物:CO2、SO2、SiO2 |
| C、混合物:铝热剂、淀粉、漂白粉 |
| D、同素异形体:C60、C70、金刚石 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com