
分析 (1)游离态的氮元素反应生成化合态氮元素为氮的固定,如工业合成氨;
(2)热化学方程式中,反应焓变=反应物的总键能-生成物的总键能,据此计算;
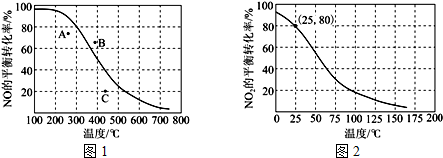
(3)①2NO(g)+O2(g)?2NO2(g),反应是气体体积减小的反应压强越大平衡正向进行,图中曲线上各点为等压不等温,通过控制变量做等温线确定ABC三点与曲线交点等温不等压,从而确定曲线以下的点压强小于100kPa,曲线以上的点压强大于100kPa;
②利用三段法列式计算,恒压100kPa、25℃时NO2的转化率为80%,设起始量二氧化氮物质的量为x,
2NO2(g)?N2O4(g)
起始量(mol) x 0
变化量(mol) 0.8x 0.4x
平衡量(mol) 0.2x 0.4x
平衡体系中N2O4的物质的量分数=$\frac{0.4x}{0.6x}$×100%=66.7%,
Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数列式计算;
(4)压缩活塞平衡正移,反应放热,针管微热,活塞固定时2NO2(g)?N2O4(g)已达平衡状态,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低,颜色变浅.
解答 解:(1)游离态的氮元素反应生成化合态氮元素为氮的固定,如工业合成氨,反应的化学方程式为:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3,
故答案为:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3;
(2)N2(g)+O2(g)$\frac{\underline{\;放电\;}}{\;}$2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ•mol-1、498kJ•mol-1、632kJ•mol-1,反应焓变△H=(946kJ•mol-1+498kJ•mol-1)-2×632kJ•mol-1=+180KJ/mol,
故答案为:+180;
(3)①图中曲线上各点为等压不等温,通过控制变量做等温线确定ABC三点与曲线交点等温不等压,从而确定曲线以下的点压强小于100kPa,曲线以上的点压强大于100kPa,所以B点压强最大,
故答案为:B;②利用三段法列式计算,恒压100kPa、25℃时NO2的转化率为80%,设起始量二氧化氮物质的量为x,
2NO2(g)?N2O4(g)
起始量(mol) x 0
变化量(mol) 0.8x 0.4x
平衡量(mol) 0.2x 0.4x
平衡体系中N2O4的物质的量分数=$\frac{0.4x}{0.6x}$×100%=66.7%,
Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,
则Kp=$\frac{100kpa×66.7%}{[100kpa×(1-66.7%)]^{2}}$
故答案为:66.7%;$\frac{100kpa×66.7%}{[100kpa×(1-66.7%)]^{2}}$;
(4)压缩活塞平衡正移,反应放热,针管微热,活塞固定时2NO2(g)?N2O4(g)已达平衡状态,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低,颜色变浅.
故答案为:变浅;活塞固定时2NO2(g)?N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.
点评 本题考查了化学键键能计算反应焓变、图象分析化学平衡影响因素、平衡常数计算,掌握化学平衡移动原理是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作及现象 | 实验结论或实验目的 |
| A | 用洁净的铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 溶液中有Na+,无K+ |
| B | 向硅酸钠溶液中滴入酚酞,溶液变红,再滴加稀盐酸,溶液红色变浅直至消失 | 非金属性:Cl>Si |
| C | 向Ba(NO3)2溶液中通入SO2,有白色沉淀产生 | SO2具有还原性 |
| D | 将含少量KNO3杂质的NaCl晶体制成热的饱和溶液,冷却结晶,过滤 | 除去NaCl中的KNO3杂质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光伏发电是将化学能转化为电能 | |
| B. | 钢铁吸氧腐蚀正极的电极反应式是O2+4e-+2H2O=4OH- | |
| C. | 通过电解NaCl水溶液的方法生产金属钠 | |
| D. | 铅蓄电池的负极材料是Pb,正极材料是PbSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个Fe(OH)3胶体粒子的质量为107g | |
| B. | 标准状况下,1L液态水中含有的H+数目为10-7NA | |
| C. | 14g分子式为CnH2n的链烃中含有的碳碳双键的数目为NA/n | |
| D. | 1 mol冰醋酸和l mo1乙醇经酯化反应可生成H2O分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化氯具有强氧化性,可用于杀菌消毒 | |
| B. | 氢氧化铝具有弱碱性,可用于治疗胃酸过多 | |
| C. | 二氧化硅的熔沸点很高,可用于制作石英坩埚 | |
| D. | 钠钾合金的密度小,可用于快中子反应堆的热交换剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
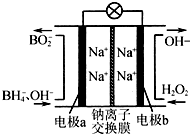 硼氢化钠(NaBH4)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图.下列说法正确的是( )
硼氢化钠(NaBH4)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图.下列说法正确的是( )| A. | 电极a为正极,b为负极 | |
| B. | 放电时,Na+从b极区移向a极区 | |
| C. | 电极b上发生的电极反应为H2O2+2e-═2OH- | |
| D. | 每生成1 mol BO2-转移6 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
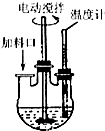 实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.
实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于5s | B. | 等于10s | C. | 大于10s | D. | 小于10s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com