
| A. | ①③④ | B. | ①②⑥ | C. | ②④⑦ | D. | ①⑤⑥ |
分析 增大浓度、构成原电池均可加快反应速率,因盐酸过量,Zn的物质的量不变时生成氢气的总量不变,以此来解答.
解答 解:①石墨、Zn、盐酸构成原电池,加快反应速率,且Zn的物质的量不变,生成氢气不变,故选;
②铜粉、Zn、盐酸构成原电池,加快反应速率,且Zn的物质的量不变,生成氢气不变,故选;
③CuO与盐酸反应,Zn置换出Cu,生成氢气减小,故不选;
④锌粒增多,生成氢气增多,故不选;
⑤Zn与CuCl2溶液置换出Cu,生成氢气减小,故不选;
⑥浓盐酸,氢离子浓度增大,且Zn的量不变,则加快反应速率,又不响产生H2总量,故选;
⑦KNO3在酸性条件下与Zn发生氧化还原反应生成NO,不生成氢气,故不选;
故选B.
点评 本题考查反应速率的比较,为高频考点,把握浓度、原电池对反应速率的影响为解答的关键,侧重分析与应用能力的考查,注意KNO3在酸性条件下强氧化性的应用,题目难度不大.


科目:高中化学 来源: 题型:实验题
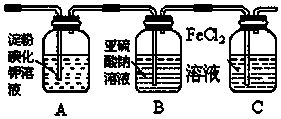
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe 2+、CH 3COOˉ、SO 42ˉ、Na + | B. | Ca 2+、K +、Cl-、HCO 3- | ||
| C. | NH 4+、Al 3+、NO 3-、Cl- | D. | K +、Na +、SO 32-、AlO 2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Y | Z | ||
| X | W |
| A. | X的最高价氧化物是碱性氧化物 | |
| B. | Z、W均可与Mg形成离子化合物 | |
| C. | 原子半径的大小顺序:r (Z)>r (Y)>r (X) | |
| D. | Y、Z、W的氧化物排放到空气中均会导致酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验目的 | 试剂及方法 |
| 证明某地雨水呈酸性 | A |
| 检验自来水中是否含有Cl- | C |
| 除去FeCl2溶液中的少量FeCl3 | B |
| 除去Fe2O3中的Al2O3 | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的干馏、石油的分馏是物理变化 | B. | 煤的液化、石油的裂化是化学变化 | ||
| C. | 天然气的主要成分是甲烷 | D. | 三者均属于不可再生的能源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com