
I、A、B、C、D、E都是短周期元素,原子半径D>C>A>E>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍,且D为金属。试回答:
(1) 在五种元素中,能形成的最简单的液态或气态氢化物的稳定性由大而小的顺序是(用具体的分子式表示)
(2) A与B形成的三原子分子的结构式是 ,B与D形成的原子个数比为1∶1的化合物的电子式是 。
(3) E的一种氢化物叫肼,其分子中E原子与氢原子个数比为1 :2。已知32克液态肼在氧气中完全燃烧生成氮气和液态水放热624KJ则该反应的热化学方程式为__________________。
(4) 肼—空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%—30%的KOH溶液。该燃料电池的正极的电极反应式是____________。
II、 现有如下两个反应:
(A)NaOH + HCl =NaCl + H2O
(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(5)根据能设计成原电池的反应选择适宜的材料和试剂设计一个原电池:
请画原电池装置示意图(注明电极正负极、电极材料、电解质溶液)
常用来冶炼该电池负极材料的两种方法是(用化学方程式表示)_________、_____。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
将锌片和铜片用导线连接后平行放入稀硫酸中,发生原电池反应,下列叙述错误的是
A.溶液的pH增大 B.溶液中的Zn2+浓度增大
C.溶液中的SO42— 浓度增大 D.溶液的密度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是
A.已知2H2(g)+O2(g) = 2H2O(g) ΔH =-483.6 kJ·mol-1,
则氢气的燃烧热为 241.8 kJ·mol-1
B.已知NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l) ΔH =-57.3 kJ·mol-1,
则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量
C.已知2C(s)+2O2(g) = 2CO2(g) ΔH=a
2C(s)+O2(g) = 2CO(g) ΔH=b,则a>b
D.已知P(白磷,s) =P(红磷,s) ΔH<0,则白磷比红磷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
为检验某卤代烃(R—X)中的X元素,有下列实验操作:①加热煮沸 ②加入AgNO3溶液 ③取少量的卤代烃 ④加入稀硝酸酸化 ⑤加入NaOH溶液 ⑥冷却。正确操作的先后顺序是( )
A.③①⑤⑥②④ B.③②①⑥④⑤ C.③⑤①⑥④② D.③⑤①⑥②④
查看答案和解析>>
科目:高中化学 来源: 题型:
氯水中存在多种微粒,下列有关粒子的表示方法正确的是 ( )
A.氯气的电子式:Cl Cl
Cl
B.氢氧根离子的电子式: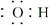
C.次氯酸分子的结构式:H—O—Cl
D.HClO的电子式: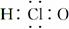
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述中正确的是
A、CS2为V形的极性分子 B、ClO3-的空间构型为平面三角形
C、SF6中的空间构型为正四面体形 D、SiF4和SO32-的中心原子均为sp3杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com