
【题目】百服宁口服液为解热镇痛药,主要用于治疗头痛、发烧.其主要化学成分的结构简式如图,下列有关该有机物的叙述正确的是( ) 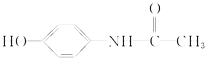
A.分子式为C8H10NO2
B.该有机物属于α﹣氨基酸
C.该有机物属于α﹣氨基酸的同分异构体有3种
D.该有机物与FeCl3溶液发生显色反应
科目:高中化学 来源: 题型:
【题目】一种用烃A合成高分子化合物N的流程如图: 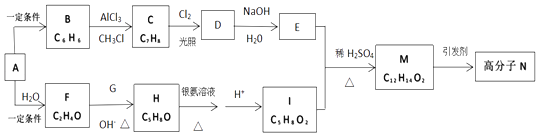
经测定烃A在标准状况下的密度为1.16gL﹣1 , F和G是同系物,核磁共振氢谱显示有机物H中有四种峰,且峰值比为3:3:1:1.
已知:
Ⅰ. ![]() →
→ 
Ⅱ. ![]()
![]() +R1Cl
+R1Cl ![]()
![]() +HCl
+HCl
Ⅲ.R1CHO+R2CH2CHO ![]() R1﹣HC=
R1﹣HC= ![]() +H2O(R1、R2、R3代表烃基或氢原子)回答下列问题:
+H2O(R1、R2、R3代表烃基或氢原子)回答下列问题:
(1)写出A的结构简式 .
(2)H中所含官能团的名称是 .
(3)H→I、M→N的反应类型分别是、 .
(4)写出F和G反应生成H的化学方程式 .
(5)E和I反应生成M的化学方程式为 .
(6)芳香族化合物Q是M的同分异构体,与M具有相同官能团,且水解可以生成2﹣丙醇,则Q的种类有种.(不考虑立体异构)
(7)请参考以上流程,依照:原料 ![]() …→产物模式,设计一个由乙烯合成2﹣丁烯醛的流程,无机试剂自选.
…→产物模式,设计一个由乙烯合成2﹣丁烯醛的流程,无机试剂自选.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用63%的浓HNO3 (其密度为1.4g/mL)配制240mL 0.50mol/L稀HNO3 , 若实验仪器有:A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒 E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯.
(1)此浓硝酸的物质的量浓度为mol/L
(2)应量取63%的浓硝酸mL,应选用 . (填仪器的字母编号)
(3)实验时还需选用的仪器有(填序号) D、I、
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号) .
①量取浓硝酸的量筒用蒸馏水洗涤2﹣3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(5)容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中移入液体时,需要一定的耐心和技巧.有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是
A.可以按此建议改进,便于使用容量瓶
B.不能按此建议改进,因为会降低容量瓶的精确度
C.不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于阿伏伽德罗常数的说法正确的是( )
A.1L0.1mol/L FeCl3溶液完全水解得到的Fe(OH)3胶体微粒数小于0.1NA
B.一定条件下的密闭容器中,6.4gSO2可被氧气氧化得到SO3的分子数为0.1NA
C.常温下18g铝放入足量浓硫酸中转移电子数2NA
D.0.1NA的NO在一密闭容器中与足量氧气完全反应,得到0.1molNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiO2在光照射下可使水分解:2H2O ![]() 2H2↑+O2↑,该过程类似植物的光合作用.下图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
2H2↑+O2↑,该过程类似植物的光合作用.下图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( ) 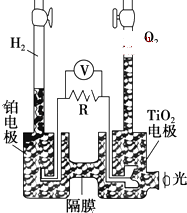
A.TiO2电极上发生的反应为:2H++2e﹣═H2↑
B.该装置工作时,TiO2电极附近溶液的pH变大
C.该装置工作时,电流由TiO2电极经R流向铂电极
D.该装置可以将光能转化为电能,同时也能将其转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.1molH2O所含有的原子数为NA
B.32gO2含有的氧原子数为2NA
C.常温常压下,11.2 LCl2 所含的分子数为0.5NA
D.1L0.1mol/LNaCl溶液中所含的Na+数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题。
(1)燃烧法是测定有机物组成的传统方法.有机物X由C、H、O三种元素组成,经测定其相对分子质量为90.取1.8g X在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g.则有机物X的分子式为 .
(2)核磁共振谱(NMR)是现代化学测定有机物结构最常用的方法之一.已知(1)中有机物X含有一个﹣COOH,在1HNMR谱上观察氢原子给出四种特征峰,强度为3:1:1:1.则X的结构简式为 .
(3)化合物A和B的分子式都是C3H6Cl2 , A的PMR谱上只有1个峰,则A的结构简式为 . B的PMR谱上有2个峰,B的结构简式为 , 写出物质B在NaOH水溶液中加热条件下反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识填空
(1)下列物质中,属于芳香族化合物的是 , 属于芳香烃的是 ,属于苯的同系物的是 .(填编号)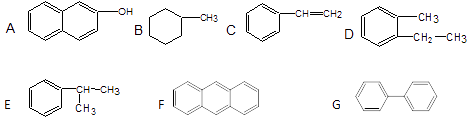
(2)已知芳香烃A是煤焦油分馏出的一种组分.A不与溴水反应,但能使高锰酸钾酸性溶液褪色.1mol A在镍催化剂的作用下,可与3mol H2发生加成反应.0.5mol A完全燃烧,生成3.5mol CO2和2mol H2O.通过计算推断A的名称是 .写出A与浓硝酸、浓硫酸混合酸在100℃时反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 .
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)4NO2(g)+O2(g);△H>0 ①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将(填“增大”、“减小”、“不变”).
②如表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1000 |
c(N2O5)/molL﹣1 | 5.00 | 3.52 | 2.48 |
则500s内N2O5的分解速率为
③在T2温度下,反应1000s时测得NO2的浓度为4.98molL﹣1 , 则T2T1(填>、<或=).
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5 , 装置如图所示,其中Y为CO2 . 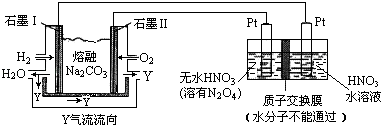
写出石墨Ⅰ电极上发生反应的电极反应式 , N2O5在电解池的区生成(填“阳极”或“阴极”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com