

| A. | 无法确定沉淀C的成分 | |
| B. | 无法确定原试液中是否含有Al3+、Cl- | |
| C. | 原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42- | |
| D. | 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+ |
分析 加入过量稀硫酸无明显变化,说明无碳酸根离子,无Ba2+,无AlO2-;
加入硝酸钡有气体,说明有亚铁离子存在且被氧化,沉淀为硫酸钡;
加入NaOH有气体,说明存在铵根离子,气体氨气,沉淀B为红褐色氢氧化铁沉淀;
通入少量CO2产生沉淀,先与OH-、Ba2+反应,沉淀C为碳酸钡,不能说明存在Al3+.
因为存在的离子浓度均为0.1mol•L-1,从电荷的角度出发,只能含有NH4+、Fe2+、Cl-、SO42-才能保证电荷守恒,K+不能存在.
解答 解:加入过量稀硫酸无明显变化,说明无碳酸根离子,无Ba2+,无AlO2-;
加入硝酸钡有气体,因为前面已经加入了硫酸,硝酸根离子在酸性条件下具有强氧化性,说明有亚铁离子存在且被氧化,沉淀为硫酸钡;
加入NaOH溶液有气体生成,说明存在铵根离子,气体为氨气,沉淀B为红褐色氢氧化铁沉淀;
通入少量CO2产生沉淀,先与OH-、Ba2+反应,沉淀C为碳酸钡,不能说明存在Al3+;
因为存在的离子浓度均为0.1mol•L-1,从电荷的角度出发,只能含有NH4+、Fe2+、Cl-、SO42-才能保证电荷守恒,K+不能存在,
A、C的成分是碳酸钡,故A错误;
B、溶液中一定含有氯离子,故B错误;
C、据以上分析知道,溶液含有NH4+、Fe2+、Cl-、SO42-,故C正确;
D、溶液含有的阳离子是NH4+、Fe2+,无钡离子,故D错误.
故选C.
点评 本题考查了常见离子的性质检验,注意硝酸根离子在酸性条件下具有强氧化性,另外本题需要根据电荷守恒判断氯离子是否存在,难度较大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题

| A. | 苯乙醇属于芳香醇,它与邻甲基苯酚互为同系物 | |
| B. | 1 mol CPAE最多可与含4 mol Br2的水溶液发生反应 | |
| C. | 用FeCl3溶液可以检测上述反应中是否有CPAE生成 | |
| D. | 咖啡酸、苯乙醇及CPAE都能发生取代、加成和消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质$\stackrel{+O_{2}}{→}$ 氧化物 $\stackrel{+H_{2}O}{→}$酸或碱$\stackrel{+NaOH或HCl}{→}$盐,能按照上述转化关系直接转化的可以是硫元素 | |
| B. | 某无色溶液中加入Ba(NO3)2溶液,再加入盐酸,沉淀不溶解,则原溶液中一定有SO42- | |
| C. | 浓硫酸有强氧化性,常温下能与Cu发生剧烈反应 | |
| D. | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 =O+RMgX→
=O+RMgX→ $\stackrel{H_{2}O}{→}$
$\stackrel{H_{2}O}{→}$ 现以乙烯和必要的无机物为原料合成2-丁醇,进而合成一种分子式为C6H8O4的具有六元环的物质J,合成线路如图,G中有两种不同化学环境的氢原子.
现以乙烯和必要的无机物为原料合成2-丁醇,进而合成一种分子式为C6H8O4的具有六元环的物质J,合成线路如图,G中有两种不同化学环境的氢原子.
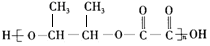 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ).下列有关它的说法不正确的是( )
).下列有关它的说法不正确的是( )| A. | 分子式为C10H16 | B. | 分子中所有碳原子可能共平面 | ||
| C. | 其一氯代物有9种 | D. | 能与溴水发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径:O2-<F-<Na+<Li+ | |
| B. | 单质的熔点:Li<Na<K<Rb | |
| C. | 分子中的键角:CH4>H2O>CO2 | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 工业上将S02转化为SO3是在接触室(如图)里进行的,中部是一个热交换器,它是用导热性能好的管状材料制成.温度低的气体从管外流过;经上层催化反应后的热气体从管内流过,通过导热材料进行气体与气体的热交换. 中学化学实验中也有许多需要进行热交换,下列实验中不需要进行热交换的是( )
工业上将S02转化为SO3是在接触室(如图)里进行的,中部是一个热交换器,它是用导热性能好的管状材料制成.温度低的气体从管外流过;经上层催化反应后的热气体从管内流过,通过导热材料进行气体与气体的热交换. 中学化学实验中也有许多需要进行热交换,下列实验中不需要进行热交换的是( )| A. | 电解水 | B. | 实验室制取少量氨气 | ||
| C. | 测定中和热 | D. | 制取乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com