
【题目】下列工业生产的反应原理不涉及氧化还原反应的是
A.铝热反应冶炼铁:Fe2O3+2Al![]() 2Fe+Al2O3
2Fe+Al2O3
B.工业上以NH3、CO2、饱和食盐水为原料生产NaHCO3:NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl
C.硝酸厂以氨气为原料制取硝酸:NH3→NO→NO2→HNO3
D.工业电解Al2O3制备金属铝:2Al2O3(熔融) 4Al+3O2↑
4Al+3O2↑
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】对于反应H2(g)+I2(g)![]() 2HI(g)
2HI(g) ![]() H<0,下列说法正确的是
H<0,下列说法正确的是
A. 反应达到平衡后,缩小容器体积,混合气体平均相对分子质量变小
B. 反应达到平衡后,保持容器温度和体积不变,充入HI气体,再次达到平衡,H2转化率减小,平衡常数K值减小
C. 若v正(H2)=2v逆(HI),反应达到平衡状态
D. 反应达到平衡后,保持容器体积不变,升温,反应体系的颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物浆液含Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图2),使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答Ⅰ和Ⅱ中的问题。

Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)反应①所加试剂NaOH的电子式为_________,B→C的反应条件为__________,C→Al的制备方法称为______________。
(2)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)___________。
a.温度 b.Cl-的浓度 c.溶液的酸度
(3)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________。
Ⅱ.含铬元素溶液的分离和利用
(4)用惰性电极电解时,CrO42-能从浆液中分离出来的原因是__________,分离后含铬元素的粒子是_________;阴极室生成的物质为___________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,碳酸钙在水中的沉淀溶解平衡曲线如图所示,已知25℃时硫酸钙的Ksp=9.1×10-6。
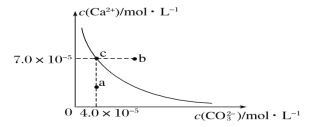
(1)通过蒸发,可使稀溶液由_______点变化到_______点。
(2)在25℃时,反应CaSO4(s)+CO32- (aq)CaCO3(s)+SO42-(aq)的平衡常数K_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁是有机合成中常用的催化剂,如图是实验室模拟化工厂利用工业废铁屑(杂质不与盐酸反应)制备催化剂氯化铁的部分装置图,下列相关说法正确的是( )
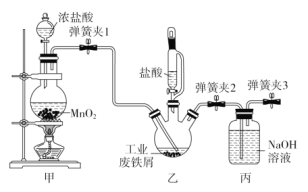
A.实验室也可以用装置甲制备SO2、C2H4
B.实验过程中,应先让装置乙中的反应进行一段时间后,再开始装置甲中的反应
C.实验过程中应该关闭弹簧夹3,让装置丙中的NaOH溶液充分吸收多余的Cl2
D.反应结束后将三颈烧瓶中的溶液加热浓缩、冷却结晶,可制得氯化铁晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000molL-1NaOH溶液滴定20.00mL 0.1000molL-1CH3COOH溶液所得滴定曲线如图:
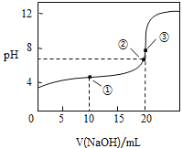
(1)在整个实验过程中,不需要的仪器是 ______ (填序号).
a.100mL容量瓶 b.锥形瓶 c.滴定管夹 d.漏斗 e.玻璃棒 f.滴定管
(2)点②所示溶液为中性:c(Na+)________c(CH3COO-)(填“>”“<”或“=”)。
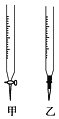
(3)盛装标准NaOH溶液选择图中滴定管_________(填标号)。
(4)滴定时边滴边摇动锥形瓶,眼睛应注意观察____________。
(5)下列操作会导致测定结果偏低的是______。
A.碱式滴定管在装液前未用标准NaOH溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(6)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4mol/L的KMnO4溶液。
Ⅰ、滴定终点的现象是_________________________________。
Ⅱ、计算:血液中含钙离子的浓度为______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体粉末甲由FeSO4、Fe2(SO4)3、CuSO4、CaCO3、SiO2、NaCl中的若干种组成,取一定量的固体甲进行如下实验:
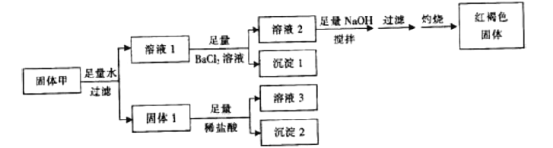
固体1质量为11g,沉淀1质量为23.3g,沉淀2质量为6g,红褐色固体质量为8g。下列说法正确的是( )
A. 溶液Ⅰ加入KSCN溶液呈红色
B. 取少量溶液2加入酸化的硝酸银溶液,生成白色沉淀,则甲中一定有NaCl
C. 固体Ⅰ与稀盐酸反应时还生成了标准状况下气体1.12L
D. 沉淀2不溶于任何酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合草酸晶体的组成可表示为![]() ,为测定x的值,做了如下实验:
,为测定x的值,做了如下实验:
![]() 称取Wg纯草酸晶体,将其配制成100mL水溶液为待测液;
称取Wg纯草酸晶体,将其配制成100mL水溶液为待测液;
![]() 取25mL待测液放入锥形瓶中,再加入适量的稀
取25mL待测液放入锥形瓶中,再加入适量的稀![]() ;
;
![]() 用浓度为a
用浓度为a![]() 的
的![]() 标准溶液进行滴定
标准溶液进行滴定![]() 滴定过程中有
滴定过程中有![]() 、
、![]() 生成
生成![]() 。
。
请回答:(1)写出滴定时发生的反应的离子方程式为:______。
(2)滴定时,将![]() 标准液装在 ______ 式滴定管中。
标准液装在 ______ 式滴定管中。
(3)假设滴定终点时,用去VmL![]() 溶液,则待测草酸溶液的物质的量浓度为 ______
溶液,则待测草酸溶液的物质的量浓度为 ______ ![]() 。
。
(4)在上述实验中,下列操作![]() 其他操作正确
其他操作正确![]() 会造成测定结果x值偏高的有 ______
会造成测定结果x值偏高的有 ______ ![]() 填字母
填字母![]() 。
。
A.滴定终点读数时俯视读数![]() 酸式滴定管使用前,水洗后未用标准液润洗
酸式滴定管使用前,水洗后未用标准液润洗
C.锥形瓶水洗后再用待测液润洗![]() 滴定时所用的
滴定时所用的![]() 溶液因久置而导致浓度变小。
溶液因久置而导致浓度变小。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚乙酯是一种重要的添加剂,其结构简式为![]() 。用环氧乙烷合成碳酸亚乙酯的反应为:
。用环氧乙烷合成碳酸亚乙酯的反应为:![]() 。下列说法错误的是
。下列说法错误的是
A.上述反应属于加成反应
B.碳酸亚乙酯的二氯代物只有两种
C.碳酸亚乙酯中的所有原子处于同一平面内
D.1mol碳酸亚乙酯最多可消耗2molNaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com