
| A. | H2XO3 | B. | HXO3 | C. | H3XO3 | D. | H2XO4 |
分析 某元素X的气态氢化物的化学式为H2X,在其氢化物中X显-2价,则X位于第VIA族,其原子最外层有6个电子,主族元素最外层电子数与其族序数相等,所以X位于第VIA族,主族元素中元素最高化合价与其族序数相等,但O、F元素除外,所以X元素最高正化合价为+6价,根据化合物中各元素化合价的代数和为0确定其最高价氧化物的水化物化学式.
解答 解:某元素X的气态氢化物的化学式为H2X,在其氢化物中X显-2价,则X位于第VIA族,其原子最外层有6个电子,主族元素最外层电子数与其族序数相等,所以X位于第VIA族,主族元素中元素最高化合价与其族序数相等,但O、F元素除外,所以X元素最高正化合价为+6价,化合物中各元素化合价的代数和为0,所以其最高价氧化物的水化物化学式为H2XO4,故选D.
点评 本题考查原子结构和元素性质,明确元素化合价与其族序数的关系式是解本题关键,注意规律中的异常现象,题目难度不大.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:解答题
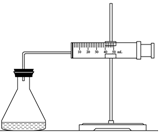 实验室用H2O2分解反应制取氧气时,常加入催化剂以加快反应速率,某研究性学习小组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应.
实验室用H2O2分解反应制取氧气时,常加入催化剂以加快反应速率,某研究性学习小组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应.| 实验编号 试剂 | A | B | C |
| 10% H2O2/mL | 20.0 | V1 | V2 |
| 2mol/L FeCl3/mL | 0 | 5.0 | 10.0 |
| H2O/mL | V3 | V4 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大理石与盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 将过量SO2通入冷氨水中:SO2+NH3•H2O=HSO3-+NH4+ | |
| D. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的硝化反应中,向浓硫酸中加浓硝酸制得混合酸 | |
| B. | 向稀氨水中逐渐加入硝酸银溶液来配制银氨溶液 | |
| C. | 向相对过量的氢氧化钠溶液中滴入少量硫酸铜溶液以配制新制氢氧化铜 | |
| D. | 溴乙烷在氢氧化钠溶液的存在下进行水解后,加入硝酸银溶液,可检验溴离子的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
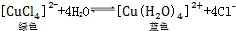 .下列措施:①加锌粉 ②加蒸馏水 ③通入HCl气体 ④浓缩.能使呈蓝色的CuCl2溶液变为绿色的是( )
.下列措施:①加锌粉 ②加蒸馏水 ③通入HCl气体 ④浓缩.能使呈蓝色的CuCl2溶液变为绿色的是( )| A. | ①② | B. | ①③ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
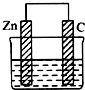 一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:
一个由锌片和石墨棒作为电极的原电池如图所示,电极反应分别是:| A. | 电子从石墨经外电路流向锌片,电解质溶液为酸性溶液 | |
| B. | 锌片是负极,石墨是正极 | |
| C. | 电池总反应为2Zn+O2═2ZnO | |
| D. | 该原电池工作一段时间后石墨附近溶液中的c(OH-)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c1:c2的值不能确定 | |
| B. | 平衡时,Y和Z的生成速率之比为1:1 | |
| C. | 0.48mol•L-1<c1+c2+c3<0.56mol•L-1 | |
| D. | c1的取值范围为0<c1<0.14 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
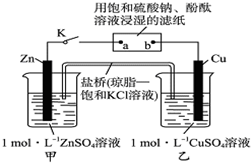
| A. | 电子沿Zn→a→b→Cu路径流动 | B. | Cu电极上发生氧化反应 | ||
| C. | 片刻后可观察到滤纸a点变红色 | D. | 片刻后甲池中c(SO42-)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每生成2molHCl放出179kJ热量 | B. | 每生成1molHCl放出179kJ热量 | ||
| C. | 每生成2molHCl吸收179kJ热量 | D. | 每生成1molHCl吸收179kJ热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com