
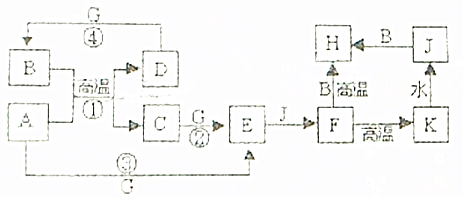
 ,D为Si,位于周期表第3周期ⅣA族,B为SiO2,为光导纤维的重要原料,
,D为Si,位于周期表第3周期ⅣA族,B为SiO2,为光导纤维的重要原料, ;第3周期ⅣA族;制造光导纤维;
;第3周期ⅣA族;制造光导纤维;
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、MgCl2(熔融)
| ||||
B、2AlCl3(熔融)
| ||||
C、HgO+CO
| ||||
D、2MgO+C
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 铅有+2和+4两种价态,铅的常见氧化物四氧化三铅(Pb2O4)和二氧化铅(PbO2)均常用于蓄电池中,回答下列问题:
铅有+2和+4两种价态,铅的常见氧化物四氧化三铅(Pb2O4)和二氧化铅(PbO2)均常用于蓄电池中,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、富含N、P元素的生活用水可以直接用来灌溉农田 |
| B、淀粉、纤维素、蛋白质、葡萄糖都是天然高分子化合物 |
| C、“地沟油”虽然对人体有害,但对“地沟油”进行分馏可制得汽油、煤油,达到变废为宝的目的 |
| D、蛋白质、油脂、蔗糖都能水解,但水解产物都不相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com