
| A. | NaHCO3溶液的电离:NaHCO3═Na++HCO3- | |
| B. | 氯化铵溶液的水解:NH4++H2O═NH3•H2O+H+ | |
| C. | 碳酸钠的水解:CO32-+2H2O═H2CO3+2OH- | |
| D. | 氯化铝和碳酸钠溶液混合:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2 |
分析 A.碳酸氢钠为强电解质,完全电离;
B.水解为微弱的,且是可逆的,应用可逆符号;
C.多元弱酸根离子分步水解,以第一步为主;
D.双水解彻底的应标注沉淀,气体符号.
解答 解:A.碳酸氢钠为强电解质,完全电离,电离方程式:NaHCO3═Na++HCO3-,故A正确;
B.氯化铵溶液的水解,离子方程式:NH4++H2O$\stackrel{.}{?}$NH3•H2O+H+,故B错误;
C.碳酸根离子是多元弱酸根离子分步水解,以第一步为主:CO32-+H2O$\stackrel{.}{?}$HCO3-+OH-,故C错误;
D.氯化铝和碳酸钠溶液混合发生双水解,离子方程式:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑,故D错误;
故选:A.
点评 本题考查了离子方程式的书写,侧重考查电解质电离方程式、盐类水解的离子方程式书写,明确电解质强弱及电离方式、熟悉盐类水解规律及水解离子方程式书写注意问题是解题关键,注意双水解彻底的应标注沉淀、气体符号.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:填空题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 叠氮化物是一类重要化合物,氢叠氮酸(HN3)是一种弱酸,如图1为分子立体结构示意图.肼(N2H4)被亚硝酸氧化时便可生成氢叠氮酸(HN3):N2H4+HNO2═2H2O+HN3.它的酸性类似于醋酸,可微弱电离出H+和N${\;}_{3}^{-}$.试回答下列问题:
叠氮化物是一类重要化合物,氢叠氮酸(HN3)是一种弱酸,如图1为分子立体结构示意图.肼(N2H4)被亚硝酸氧化时便可生成氢叠氮酸(HN3):N2H4+HNO2═2H2O+HN3.它的酸性类似于醋酸,可微弱电离出H+和N${\;}_{3}^{-}$.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
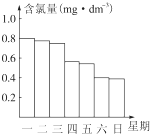 某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.
某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | |
| 第一次称量 | 第二次称量 | ||
| 11.710g | 22.700g | 18.621g | a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某温度下,溶液中c(H+)=10xmol•L-1,c(OH-)=10ymol•L-1,x和y的关系如图所示.则该温度下,0.01mol•L-1的NaOH溶液的pH为( )
某温度下,溶液中c(H+)=10xmol•L-1,c(OH-)=10ymol•L-1,x和y的关系如图所示.则该温度下,0.01mol•L-1的NaOH溶液的pH为( )| A. | 10 | B. | 11 | C. | 13 | D. | 12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol某气体的体积为22.4L,该气体所处的状态一定是标准状况 | |
| B. | 将22.4L氯化氢气体溶解于水并配成1L溶液,所得溶液浓度为1mol•L-1 | |
| C. | 任何状况下,1molCO2和18gH2O所含的分子数和原子数都相等 | |
| D. | 20ml0.1mol/L的AlCl3溶液中的Cl-的物质的量浓度小于50mL0.2mol/L的NaCl溶液中的Cl-的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| B. | 溶于水后能电离出氢离子的化合物一定是酸 | |
| C. | 硫酸钡难溶于水,故硫酸钡不属于电解质 | |
| D. | 二氧化碳溶于水能导电,但二氧化碳不属于电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com